Гастроэнтеростомия при раке желудка
При раке желудка выполняют два типа паллиативных операций. При первом типе вмешательств операция, не устраняя очага поражения, направлена на улучшение питания и общего состояния больного. Такими операциями являются обходной анастомоз между желудком и тонкой кишкой – гастроэнтероанастомоз, гастро- и еюностомии. При втором типе операций удаляется первичный очаг опухоли или метастазы. К таким операциям относятся паллиативные резекции, паллиативные гастрэктомии и удаление метастазов.
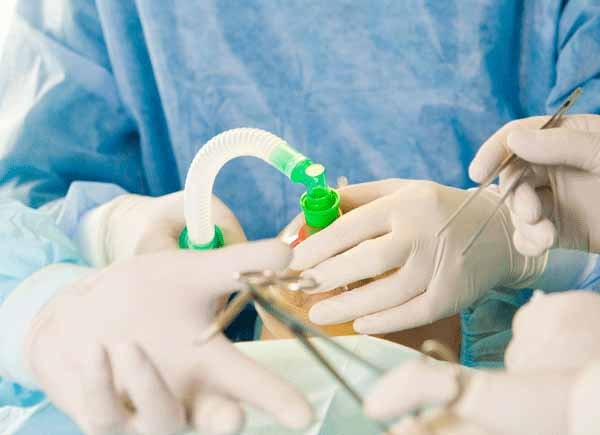
Гастроэнтеростомия (наложение гастроэнтеростомоза)
Желудочно-кишечный анастомоз накладывается при иноперабельном раке выходного отдела желудка, и эта операция является наиболее частым паллиативным вмешательством. Смысл операции заключается в создании соустья между желудком и тощей кишкой. В настоящее время выполняют заднюю – позадиободочную, реже переднюю – впередиободочную гастроэнтеростомию. В первом случае через отверстие в брыжейке поперечно-ободочной кишки выводят заднюю стенку желудка и соединяют анастомозом с петлей тонкой кишки. Во втором варианте, петлю кишки проводят впереди от поперечно-ободочной кишки, прикладывают к передней стенке желудка и соединяют с ним соустьем. В 8-10 см ниже гастроэнтероанастомоза обычно накладывается межкишечный брауновский анастомоз.
Гастростомия
Операцию применяют при неоперабельном раке проксимального отдела желудка и пищевода, сопровождающемся нарушением проходимости пиши. Предложено более ста модификаций этой операции. Наибольшее распространение получила гастростомия по Кадеру и Витцелю.
Энтеростомия
Кишечный свищ или энтеростому накладывают для обеспечения питания больного при раке желудка и создания проходимости пищеварительного тракта. Операция также производится при обширном поражении желудка с нарушением проходимости и невозможности наложить гастростому. Подобная операция является единственным средством помочь неоперабельному больному раком резецированного желудка. Чаще искусственный свищ создается в начальном отделе кишечника (еюностомия).
Однако еюностомия не пользуется популярностью среди хирургов. Это связано с тем, что введение зонда, значительно суживающего просвет кишки, вызывает застой и создает условия для вытекания кишечного содержимого.
Ко второму типу паллиативных операций относятся паллиативные резекции. Эти операции, в основном, выполняются при невозможности полного удаления метастазов в лимфатических узлах или в органах при удалимости первичной опухоли. Паллиативную резекцию желудка производят главным образом в целях увеличения эффективности последующей лучевой и химиотерапии.
Противопоказаниями к проведению паллиативной резекции являются: метастазы в брюшину, брыжейку, сальник, асцит; отдаленные метастазы в кости, головной мозг, легкие и т.д., тяжелое общее состояние больного.
Паллиативное удаление первичного очага позволяет уменьшить массу опухоли и, тем самым, снизить токсическое ее влияние на организм больного, устранить источник непроходимости и кровотечения, что позволяет больному жить некоторое время с метастазами. В основном паллиативные резекции выполняются с целью дальнейшего проведения химио- и лучевой терапии Обходные анастомозы, гастро- и еюностомы также облегчают проведение лекарственного лечения, поскольку ослабленный голодом больной не в состоянии выдержать лечение. Улучшение состояния пациента после начала питания через стому в дальнейшем позволит применить химиотерапию. Техника таких операций такая же, как и обычной резекции желудка, но без удаления лимфатических узлов или метастазов.
Отдаленные результаты хирургического лечения рака желудка зависят от стадии заболевания, гистологической структуры опухоли и своевременности начатого лечения. При начальных формах рака 5-летняя выживаемость составляет в среднем свыше 90 %, 10-летняя – 75 %. Однако более половины пациентов раком желудка поступают на лечение в запущенном состоянии, когда радикальная операция возможна лишь у 30-40 % всех больных. В целом при экспансивном раке 5-летняя выживаемость достигает 40-45 %, при инфильтративном – 3-5 %. Наличие метастазов или прорастание серозной оболочки желудка в 2-3 раза ухудшает результаты. После гастрэктомии и проксимальной резекции 5 лет живут 20-25 % радикально оперированных. Средняя продолжительность жизни больных после радикальной операции по поводу осложненного перфорацией и кровотечением рака составляет до 30 месяцев.
Неудовлетворительные результаты хирургического метода лечения рака желудка явились предпосылкой к разработке комбинированного метода лечения. Резекция желудка или гастрэктомия производится в сочетании с лучевым или химиотерапевтическим воздействием на опухоль в пред- или послеоперационном периоде. Однако высокая радиорезистентность рака желудка ограничивает применение лучевой терапии. Лучевую терапию рака желудка в основном проводят при локально контролируемых формах – при кардиальном и кардиоэзофагеальном раке, при котором риск развития лучевого повреждения относительно невелик и предсказуем. Предоперационное облучение по интенсивной методике может увеличить количество радикальных вмешательств и показатели 5-летней выживаемости.
Наиболее эффективными препаратами при лечении больных раком желудка являются 5-фторурацил, митомицин С, адриамицин, этопозид, препараты платины. В большинстве случаев рак желудка также является химиорезистентнои опухолью, а системная внутривенная химиотерапия больных раком желудка в настоящее время не имеет перспектив в связи с низкой концентрацией препаратов в опухоли. Поэтому важным подходом при лечении больных раком желудка являются способы введения и доставки химиопрепаратов к опухолевому очагу. Наиболее адекватным путем доставки химиопрепаратов к раковой опухоли является их прямое введение в сосуды, питающие опухоль, через катетер, установленный в правой желудочно-сальниковой или левой желудочной артерии. Такая терапия, называемая внутриартериальной неоадъювантной полихимиотерапией (ВАПХТ), может выполняться не только на предоперационном этапе лечения, но и у неоперабельных больных. При сравнении эффективности лечения больных раком желудка оказалось, что наибольшая, 10-летняя, выживаемость была достигнута при применении селективной ВАПХТ с последующей операцией (64 %) и практически не менялась при системной химиотерапии с последующей операцией и только лишь хирургическом лечении (28 %).
При лечении рака желудка также могут быть использованы методы непосредственного ввеедения цитостатиков в опухоль и вокруг нее во время фиброгастроскопии, внутрибрюшинно при лапароскопиях и во время выполнения радикальной операции.
Очень важное значение для повышения чувствительности раковых клеток к химио- и лучевой терапии имеет использование модифицирующих факторов. К методам, усиливающим воздействие химиопрепаратов у больных раком желудка, относится локальная гипертермия. Локальное прогревание рака желудка (СВЧ-гипертермия) при температуре 43-44°С вызывает повреждение резистентных опухолевых клеток, не относящихся к пролиферативному пулу или находящихся в зоне гипоксии ткани, не затрагивая нормальные клетки. К модификаторам химио- и лучевой терапии следует отнести действие вихревых магнитных полей, сверхнизких температур, иммунотерапию (препараты производные интерлейкинов и интерферона), использование искусственной гипергликемии. В настоящее время предложена большая группа модификаторов различного механизма действия – левамизол, лейковорин, интерферон, Т-активин, церулоплазмин, курантил, амфотерицин, циметидин, дрожжевые полисахариды, антиоксидантные комплексы, энзимы, фитоадаптогены. Благодаря адекватной доставке химиопрепаратов к опухоли и применению модуляторов, при лечении рака желудка становится вполне возможным перевод рака желудка из «нерезектабельного» в «резектабельное» состояние.
Источник
При раке желудка выполняют два типа паллиативных операций. При первом типе вмешательств операция, не устраняя очага поражения, направлена на улучшение питания и общего состояния больного. Такими операциями являются обходной анастомоз между желудком и тонкой кишкой – гастроэнтероанастомоз, гастро- и еюностомии. При втором типе операций удаляется первичный очаг опухоли или метастазы. К таким операциям относятся паллиативные резекции, паллиативные гастрэктомии и удаление метастазов.
Гастроэнтеростомия (наложение гастроэнтеростомоза)
Желудочно-кишечный анастомоз накладывается при иноперабельном раке выходного отдела желудка, и эта операция является наиболее частым паллиативным вмешательством. Смысл операции заключается в создании соустья между желудком и тощей кишкой. В настоящее время выполняют заднюю – позадиободочную, реже переднюю – впередиободочную гастроэнтеростомию. В первом случае через отверстие в брыжейке поперечно-ободочной кишки выводят заднюю стенку желудка и соединяют анастомозом с петлей тонкой кишки. Во втором варианте, петлю кишки проводят впереди от поперечно-ободочной кишки, прикладывают к передней стенке желудка и соединяют с ним соустьем. В 8-10 см ниже гастроэнтероанастомоза обычно накладывается межкишечный брауновский анастомоз.
Гастростомия
Операцию применяют при неоперабельном раке проксимального отдела желудка и пищевода, сопровождающемся нарушением проходимости пиши. Предложено более ста модификаций этой операции. Наибольшее распространение получила гастростомия по Кадеру и Витцелю.
Энтеростомия
Кишечный свищ или энтеростому накладывают для обеспечения питания больного при раке желудка и создания проходимости пищеварительного тракта. Операция также производится при обширном поражении желудка с нарушением проходимости и невозможности наложить гастростому. Подобная операция является единственным средством помочь неоперабельному больному раком резецированного желудка. Чаще искусственный свищ создается в начальном отделе кишечника (еюностомия).
Однао еюностомия не пользуется популярностью среди хирургов. Это связано с тем, что введение зонда, значительно суживающего просвет кишки, вызывает застой и создает условия для вытекания кишечного содержимого.
Ко второму типу паллиативных операций относятся паллиативные резекции. Эти операции, в основном, выполняются при невозможности полного удаления метастазов в лимфатических узлах или в органах при удалимости первичной опухоли. Паллиативную резекцию желудка производят главным образом в целях увеличения эффективности последующей лучевой и химиотерапии.
Противопоказаниями к проведению паллиативной резекции являются: метастазы в брюшину, брыжейку, сальник, асцит; отдаленные метастазы в кости, головной мозг, легкие и т.д., тяжелое общее состояние больного.
Паллиативное удаление первичного очага позволяет уменьшить массу опухоли и, тем самым, снизить токсическое ее влияние на организм больного, устранить источник непроходимости и кровотечения, что позволяет больному жить некоторое время с метастазами. В основном паллиативные резекции выполняются с целью дальнейшего проведения химио- и лучевой терапии Обходные анастомозы, гастро- и еюностомы также облегчают проведение лекарственного лечения, поскольку ослабленный голодом больной не в состоянии выдержать лечение. Улучшение состояния пациента после начала питания через стому в дальнейшем позволит применить химиотерапию. Техника таких операций такая же, как и обычной резекции желудка, но без удаления лимфатических узлов или метастазов.Химиотерапию в чистом виде применяют только при неоперабельных формах рака. Попытки продлить жизнь этих больных с помощью полнили монохимиотерапии показали эффективность 5-фторурацила и фторафура. 5-Фторурацил вводят внутривенно из расчета 15 мг/кг через день в суммарной дозе на курс лечения 4—5 г. Фторафур назначают по 30 мг/кг внутривенно или внутрь, рекомендуется суточную дозу делить на 2 приема, ориентировочная суммарная доза — 20—30 г. Повторные курсы химиотерапии проводят через 4—6 нед.
Химиотерапия позволяет добиться частичной регрессии опухоли у 20—30% больных. Средняя продолжительность жизни больных, перенесших паллиативную дистальную резекцию желудка, при проведении им химиотерапии составляет 23,3±3,6 мес, а если химиотерапия не назначалась — только 12,9±2,8 мес.
Профилактическая химиотерапия может проводиться у радикально оперированных больных раком желудка. Дополнительное лечение 5-фторурацилом в дозе 15 мг/кг через день (по 3 г суммарно) назначают через 1 и 3 мес после радикальной операции. Это лечение уменьшает частоту рецидивов и метастазов.
Химиотерапия перечисленными препаратами может сопровождаться рядом побочных явлений, среди которых основное значение имеет угнетение кроветворения (особенно белого ростка и тромбоцитов) и поражение слизистых оболочек желудочно-кишечного тракта. В этих случаях ограничивается возможность длительного лечения или применения высоких доз.
Источник
Паллиативные операции при раке желудка включают в себя симптоматические операции, временно облегчающие состояние пациентов, и направленные на устранение тех или иных тяжелых или опасных для жизни симптомов онкологического заболевания, а также циторедуктивные операции, которые существенно уменьшают размер первичной опухоли и метастазов, уменьшая степень опухолевой интоксикации.
В каких ситуациях проводятся паллиативные операции при раке желудка?
В лечении рака желудка главная роль до сих пор принадлежит хирургическому методу, однако, на поздних стадиях рака желудка при распространенных поражениях окружающих тканей с вовлечением регионарных лимфатических узлов и наличием отдалённых метастазов, тяжелом состоянии пациента, проведение радикальных операций невозможно. Радикальные операции при раке желудка (субтотальная резекция желудка, гастрэктомия, проксимальная резекция) – это всегда обширные операции, которые помимо вмешательства собственно на желудке сопровождаются удалением большого и малого сальника, а во время комбинированных операций одновременно удаляют полностью или частично пораженные раковым процессом соседние органы (поджелудочную железу, печень, поперечно-ободочную кишку, селезенку).
Радикальная операция при раке желудка является серьезным хирургическим вмешательством, которое требует существенной компенсации функций организма. Многим больным отказывают в операции из-за высокой степени операционного риска. Между тем при раке желудка на 4-й стадии на фоне специфической терапии 5-летняя выживаемость достигает 15-20%, а с развитием высокотехнологичных методов лечения можно рассчитывать и на большее продление жизни пациентов. Поэтому сейчас активно разрабатываются хирургические методики, позволяющие облегчить состояние и значительно улучшить качество жизни пациентов с раком желудка, радикальная операция у которых невозможна.
Выполнение паллиативных операций у пациентов с раком желудка делают возможным проведение лучевой и химиотерапии, введение индивидуальных противоопухолевых вакцин и моноклональных антител (SU11248), что позволяет добиться стойкой стабилизации течения заболевания и увеличить ожидаемую продолжительность жизни.
Когда необходимо паллиативное хирургическое вмешательство?
Диагноз 4 стадии рака желудка устанавливается при инвазивном поражении опухолью соседних органов, близлежащих лимфатических узлов, или при наличии метастазов в отдаленные органы и ткани. Хирургическое лечение в таких ситуациях применяется преимущественно для лечения жизнеугрожающих состояний – кровотечения из опухоли, прободения (перфорации) стенки желудка, стенозе желудка с развитием тяжелых водно-электролитных расстройств и невозможностью питания, желтухе при поражении опухолью печени и желчевыводящих путей.
Кровотечение из опухоли при ее распаде или в результате воздействия на нее желудочного сока проявляется нарастающей слабостью, головокружением, вплоть до потери сознания из-за снижения артериального давления, рвотой чистой кровью (со сгустками или без), или так называемой «кофейной гущей» из-за воздействия желудочного сока на компоненты крови. При длительно существующей кровопотере слабость нарастает постепенно в течение нескольких дней или недель, одновременно бледнеют видимые слизистые рта, глаз, снижается или полностью исчезает аппетит. При относительно длительном (в течение нескольких дней) кровотечении может возникать позыв к дефекации с отхождением черного полужидкого или жидкого дегтеобразного (так называемая «мелена») стула.
Кровотечение из опухоли может развиться внезапно, или нарастать постепенно, что определяется степенью распространенности опухолевого процесса и вовлечения в него крупных артериальных сосудов, проходящих вдоль малой и большой кривизны желудка. Во многих случаях пациенты с раком желудка находятся в это время дома после окончания очередного курса лучевой или химиотерапии. В ожидании «скорой помощи» необходимо уложить больного в постель и приложить к животу грелку со льдом.
В хирургическом стационаре лечение начинают с попытки остановки кровотечения с помощью кровоостанавливающих средств и установке зонда Блэкмора для прекращения желудочного кровотечения. Одновременно начинается инфузия препаратов плазмы крови с целью профилактики ДВС-синдрома, а при массивной кровопотере также проводится переливание эритроцитарной массы. Малоинвазивные вмешательства выполняются с целью поиска источника кровотечения и точечной ликвидации кровотечения, для чего проводится эндоскопическое вмешательство, позволяющее выполнить клипирование и прошивание кровоточащего сосуда, провести электро- или плазменную коагуляцию. Все эти методики остановки желудных кровотечений при раке желудка и других осложнениях онкологических заболеваний используются в Европейской онкологической клинике.
При неэффективности предпринятых мер по устранению желудочного кровотечения проводится экстренная хирургическая операция.
Перфорация (прободение) стенки желудка является одним из наиболее грозных состояний, связанных с раком желудка 4 стадии, требующей неотложного хирургического лечения. Перфорация желудка проявляется очень сильной, так называемой «кинжальной болью» в верхней трети живота с тошнотой, рвотой, сухостью во рту может свидетельствовать о появлении сквозного отверстия в стенке желудка, через которое содержимое желудка попадает в брюшную полость и вызывает сильное воспаление – перитонит.
Серьезными осложнениями рака желудка на 4 стадии заболевания, возникающими при сдавлении крупных сосудов метастатическими очагами, являются сдавление нижней полой вены, воротной вены печени, а также «механическая желтуха», обусловленная сдавлением желчных протоков.
Основным признаком «механической желтухи» является окрашивание в желтый цвет кожных покровов, склер глаз и слизистых оболочек из-за повышения в крови уровня билирубина (гипербилирубинемия). Высокий уровень билирубина опасен для жизни, поскольку приводит к развитию так называемой печеночной энцефалопатии и угнетению всех регуляторных центров головного мозга.
Желтуха – прямое противопоказание для проведения плановых химио- и лучевой терапии. Единственным радиальным методом снижения высокого уровня билирубина является восстановления оттока желчи из печени путем проведения рентгенохирургического вмешательства. Дренирование позволяет наладить временный отток наружу на поверхность кожи (наружный дренаж) или как наружу, так и в естественном направлении в кишечник (наружно-внутренний дренаж). В некоторых случаях, когда опухолевое сдавление изолирует несколько разных сегментов желчного дерева, например, как левую, так и правую доли печени, может потребоваться установка нескольких дренажей.
После снижения уровня билирубина до нормальных величин и уменьшения явлений холангита дренаж заменяется на стент или стенты – специальные эндопротезы, которые поддерживают желчный проток в открытом состоянии. Выполнение одномоментного дренирования и стентирования проводится только по строгим медицинским показаниям, чаще всего эти операции разделены по времени. В целом, дренирование и стентирование желчных протоков существенно улучшает качество жизни больных.
У 10-15% пациентов раком желудка развивается требующий хирургического вмешательства стеноз (сужение просвета) кардиального или пилорического отдела желудка. Симптомами этого состояния служат затруднение при проглатывании пищи при поражении верхних (кардиальных) отделов, тяжесть, чувство переполнения и рвота давно съеденной пищей при вовлечении перехода из желудка в 12-перстную кишку(пилоростеноз).
Стеноз при раке желудка чреват развитием опасных для жизни водно-электролитных расстройств и усугублением кахексии (истощения). Для восстановления прохождения пищи по желудочно-кишечному тракту, коррекции и профилактики водно-электролитных нарушений при иноперабельном раке желудка со стенозом пилорического отдела проводят операцию гастроэнтеростомии, т.е. наложение соустья между желудком и тощей кишкой.
C целью коррекции стеноза при неоперабельном раке проксимального (кардиального) отдела желудка c переходом на пищевод при нарушении прохождения пищи может использоваться стентирование желудка – установка специальных стентов, которые восстанавливают нормальное прохождение пищи через желудок в кишечник. Альтернативным способом хирургического лечения является наложение гастростомы – гастростомия – формирование отверстия в желудке и передней брюшной стенке, для обеспечения питания больного через зонд. В результате уменьшаются симптомы интоксикации и обеспечение питание больного.
Операции раке с метастазами
Рак желудка в большинстве случаев довольно рано дает метастазы. Из числа наиболее часто поражаемых метастазами органов следует указать печень, поджелудочную железу, легкие, яичники (метастаз Крукенберга), а также брюшину, которая покрывается множественными раковыми узелками, что сопровождается выпотом жидкости в брюшную полость (асцитом). Помимо того, что метастазы могут приводить к развитию острых осложнений, требующие экстренной хирургической помощи (сдавление нижней полой вены), они существенно нарушают функционирование пораженных органов, значительно ухудшают общее состояние, нередко сопровождаясь нестерпимыми болями, требующими постоянного обезболивания.

Как в ведущих, в т.ч. зарубежных клиниках, так и в Европейской онкологической клинике для лечения метастазов рака желудка, в частности в печень, используется чрескожная чреспеченочная радиочастотная абляция (РЧА) – методика, вызывающая контролируемый асептический некроз метастатического очага, без повреждения окружающих тканей. Результатом такого некроза становится полная гибель опухолевых клеток метастаза. При ее выполнении, которое проводится под общим обезболиванием, под ультразвуковым контролем сквозь кожу вводится монополярный радиоволновой электрод, разогревающий именно нужный участок печени и вызывающий локальный некроз метастаза. РЧА может также проводится во время открытой операции на желудке и органах брюшной полости. РЧА метастазов печени дает возможность надолго продлить жизнь пациента без возникновения рецидивов. У нас накоплен опыт неодократного проведения РЧА для полного устранения множества мелких метастазов печени, а также в случае появления новых метастатических очагов.
В отделении интервенционной онкологии и эндоваскулярной хирургии Европейской онкологической клиники выполняется химиоэмболизация артерий, питающих крупные метастазы, преимущественно в печени, с целью уменьшения негативного влияния метастазов рака на организм пациента. Прекращение кровотока в опухоли уже само по себе оказывает лечебное воздействие. Одновременная доставка в ткань опухоли химиопрепаратов разрушает ее изнутри, избавляя пациента от токсического действия лекарства на весь организм в целом.
В мире используется также такая методика лечения метастазов печени, как радиоэмболизация метастазов рака желудка в печень. Она проводится под контролем ангиографа с помощью внутрисосудистой селективной катеризации сосудов печени. В сосуд, питающий опухоль, вводятся эмболизирующие частицы с радиоактивным изотопом иттрий-90, которые в последующие после операции 64 часа продолжают изнутри воздействовать на опухоль. К сожалению, в нашей стране данная методика не доступна. Для этих целей мы направляем пациентов в клиники Израиля и Германии.
Малотравматичные резекции печени, включая радиочастотную аблацию метастазов рака в печень, в нашей клинике проводятся учеником профессора, д.м.н. Юрия Ивановича Патютко, заместителем главного врача клиники, к.м.н. Андреем Львовичем Пылёвым. Кроме того, наиболее сложные операции выполняются самим Юрием Ивановичем Патютко, руководителем хирургического отделения опухолей печени РОНЦ им. Н. Н. Блохина.
При распространении опухолевого процесса – диссеминации метастазов опухоли желудка по брюшине (т.н. канцероматоз брюшины) может происходить накопление жидкости в брюшной полости. Это состояние называется асцит, оно довольно мучительно для пациента. В основном, оно обусловлено механическим препятствием обратному всасыванию жидкости из брюшной полости, в норме происходящему очень интенсивно (до 1,5 л в сутки) и закупоркой лимфатических сосудов. При метастатическом поражении паренхимы печени, в основе развития асцита лежит, кроме того, препятствие венозному оттоку крови.
Нарушения регуляции водно-солевого обмена способствуют возникновению и нарастанию асцита. В зависимости от объема жидкости в брюшинной полости появляются те или иные расстройства и жалобы. До 1 л асцитической жидкости обычно можно обнаружить только при ультразвуковом исследовании. Большее количество проявляется увеличением и деформацией живота, который при вертикальном положении больного выглядит отвисшим, а в горизонтальном распластанным, «лягушачим». С увеличением количества жидкости нарастают чувство тяжести и тупые ноющие боли в животе. Затем развивается затруднение дыхания, появляются тошнота, отрыжка, нарушения стула, нарушение мочеиспускания, уменьшение количества отделяемой мочи, может сформироваться пупочная грыжа.
Когда жидкости становится больше 5 л и больше сдавление внутренних органов, нарушение экскурсии диафрагмы, повышение внутрибрюшного давления приводят к смещению органов вверх, в грудную полость, вызывают дыхательную недостаточность и нарушение нормального крово- и лимфотока. При этом создаются благоприятные условия для быстрого и обширного метастазирования опухоли. Однако одномоментное удаление большого количества асцитической жидкости может привести к возникновению тяжелых осложнений, поэтому в Европейской онкологической клинике для дренирования асцитов применяются современные методики лапароцентеза с использованием специальных помп для постепенного и дозированного удаления серозной жидкости.
Параллельно проводится инфузионная терапия для коррекции водно-электролитных нарушений, инфузии альбумина, коллоидов и объёмо-замещающих растворов. Для предотвращения возникновения асцита, после первичной эвакуации асцитической жидкости, мы активно используем цитостатические препараты, т.е. лекарственные вещества, способствующие уменьшению объема выпота и более медленному накоплению жидкости, в том числе внутриполостное введение лекарственных препаратов. Внутриполостная химиотерапия эффективна в 40-60% случаев и позволяет сохранить положительный эффект брюшинной пункции на срок более 2 месяцев. Лапароцентез производится под ультразвуковой навигацией и при необходимости завершается установкой дренажа для длительной эвакуации жидкости.
Применяемые в нашей клинике катетеры не ограничивают естественную двигательную активность и обеспечивают возможность возвращения пациента к привычной деятельности. При рефрактерных и массивных асцитах возможно проведение паллиативных операций (установка перитонеовенозного шунта, частичная деперитонизация стенок брюшной полости, оментогепатофренопексия и другие). При таком комплексном подходе процедуру лапароцентеза требуется делать в 2-3 раза реже, чем при классическом проведении пункции брюшинной полости.
Насколько оправданы вмешательства в 4 стадии рака желудка, ведь они не приводят к излечению?
Философия оказания медицинской помощи в Европейской онкологической клинике заключается в том, что пациенту надо стараться помочь всегда. Человеческая жизнь бесценна, и ее нужно продлить на максимально больший срок при поддержании максимально возможного качества жизни. Вмешательства на поздней стадии онкологического заболевания, включая 4-ю стадию рака желудка, должны предприниматься, поскольку они позволяют существенно улучшить качество жизни пациентов, уменьшить интоксикацию и выраженность болевого синдрома, продлить жизнь и возможность общения с родными и близкими на существенный срок. Например, проведение перитонэктомии в сочетании с гипертермической внутрибрюшной химиотерапией у больных с канцероматозом брюшины при раке желудка позволяет увеличить продолжительность жизни до 18 месяцев. При единичных изолированных метастазах рака желудка в печень ее резекция позволяет достичь 5-летней выживемости у 18–34% больных.
Для лечения 4 стадии рака желудка в отделении паллиативной и симптоматической терапии используются все возможные варианты лечения онкологических больных: все виды химиотерапии, лучевая терапия, которая позволяет уменьшать болевой синдром, а также выполняются паллиативные операции. С целью облегчения введения препаратов возможна имплантация венозных и артериальных инфузионных порт-систем для химиотерапии, проводится регионарная интраартериальная инфузия химиопрепаратов, местная терапия.
— Необходима ли какая-либо особая подготовка для проведения паллиативных операций?
Безусловно, из-за тяжести болезни наши пациенты требуют особенно тщательной подготовки и ведения послеоперационного периода. Обычно предоперационная подготовка заключается в общеукрепляющем лечении, инфузионной терапии белковыми препаратами, солевыми и коллоидными растворами, витаминами, в применении тонизирующих средств. Существуют методики предоперационной инфузионной подготовки, позволяющие уменьшить кровопотерю в процессе операции, они активно используются в нашей клинике. Как правило больные нуждаются в гипералиментации – введении питательных веществ высокой энергетической ценности.
В послеоперационном периоде на несколько дней исключают прием пищи и воды через рот. Необходимые количества жидкости и питательных веществ восполняют путём внутривенных вливаний питательных растворов с инсулином, витаминами, а также крови и белковых препаратов. Пациенту назначают антибиотики, сердечные средства, наркотики и кислород. Важным компонентом является тщательный уход, дыхательная гимнастика, внимательное наблюдение за течением послеоперационного периода. В дальнейшем огромное значение имеет правильное сбалансированное дробное питание, приём необходимых препаратов и уход за больным.
Источник
