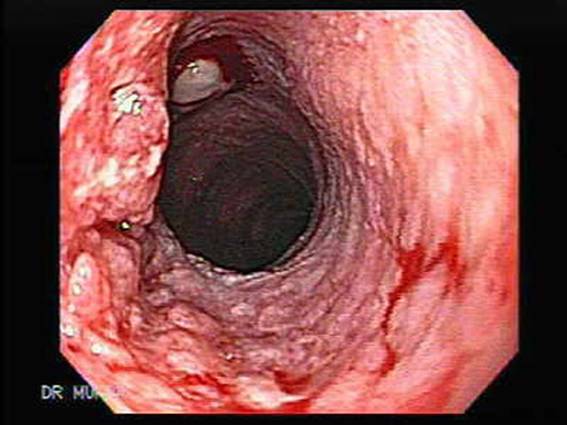
Скрининг рака желудка пищевода
«Единственной возможностью успешного лечения рака является выявление его на ранней стадии. Для этого необходимо проведение скрининга рака органов пищеварения с использованием самой современной эндоскопической техники»
проф. Нечипай А.М.
В каких случаях человеку нужно пройти гастроскопию?
«Если назначил врач. Если появились боли в желудке, изжога, другие признаки заболеваний», — примерно так многие ответят на этот вопрос. Но иногда, даже если симптомы появились недавно, бывает уже поздно.
Рак желудка, как и многие злокачественные опухоли, на ранних стадиях не проявляется никакими симптомами. Человека ничего не беспокоит, и он уверен, что здоров. Естественно, за помощью в больницу он не обращается. А ведь именно в это время лечение могло бы быть наиболее эффективным.
Зачастую, когда человека начинает что-то беспокоить, он обращается к врачу и проходит обследование, оказывается, что опухоль уже начала прорастать в соседние органы или дала метастазы. Это ухудшает прогноз.
Какова реальная ситуация в настоящее время? Наиболее красноречиво об этом расскажут цифры:
- Во время диагностики лишь у 1 из 100 больных выявляют рак желудка на I стадии. А ведь прогнозы в это время наиболее благоприятны: в течение 5 лет выживают 8 больных из 10.
- Еще у 6 из 100 обследованных людей с раком желудка выявляют II стадию. В течение 5 лет выживают 5 пациентов из 10.
- У 14–15 человек из тех же ста обнаруживают III стадию опухоли. В течение 5 лет выживает лишь 2–4 пациента из 10.
- У оставшихся 80 из 100 больных обнаруживается рак желудка IV стадии. И если такой больной проживет хотя бы 2 года с момента установления диагноза — результат считается хорошим.
Что такое скрининг?
Скрининг — это исследование, во время которого обследуют всех людей из определенной группы, несмотря на то, что у них отличное самочувствие, и они считают себя абсолютно здоровыми. Иными словами, скрининг — это профилактическое обследование. Оно помогает выявить болезни на ранних стадиях, начать своевременное лечение. А при онкологических и других опасных заболеваниях — спасти жизни многим людям.
Гастроскопия — процедура, которая занимает, как правило, 15 минут. Она не требует специальной подготовки (если не считать того, что с утра в день исследования нельзя есть и пить) и госпитализации в стационар. При этом гастроскопия имеет неоценимое значение в диагностике ранних стадий рака и предраковых состояний желудка.
Почему стоит пройти гастроскопию?
Показательным является пример Японии — страны, в которой в 1963 году был введен массовый скрининг рака желудка. В Европе и США сейчас 80% пациентов поступают на лечение с раком желудка на IV стадии, и лишь 5%-10% — на ранних стадиях. В Японии у 50% больных опухоль находится на ранних стадиях. Кроме того, в Японии средняя пятилетняя выживаемость пациентов с раком желудка составляет 53% — это один из самых высоких показателей в мире (во многих других странах — 20%-30%).
В онкологии скрининговые эндоскопические исследования проводятся главным образом для выявления ранних стадий рака и предопухолевых состояний верхнего отдела пищеварительной системы (пищевод, желудок и двенадцатиперстная кишка — эзофагогастродуоденоскопия), толстого кишечника (колоноскопия). Взрослым людям, особенно старшего возраста, эти исследования рекомендуется проходить раз в год.
В Европейской клинике гастроскопию и колоноскопию можно пройти по отдельности или в составе комплексного профилактического обследования Cancer-check, которое также включает анализы крови, рентген, КТ, УЗИ, дерматоскопию, функциональные, цитологические и генетические исследования.
Источник
На ранних стадиях рак желудка может не доставлять дискомфорта и никак не проявляться, поэтому важной мерой профилактики становится онкоскрининг. Скрининг рака желудка – это обследование, которое проводится регулярно даже в отсутствие симптомов, оно позволяет не упустить опасное заболевание в зачатке и не потерять время. В 80% случаев рак желудка, обнаруженный на I стадии, излечим.
Массово скрининговую диагностику желудка в нашей стране не проводят, но со своим лечащим врачом всегда можно согласовать индивидуальный график обследования и придерживаться его. Рассмотрим, какие методы скрининга существуют, как проходит диагностика в клинике MedEx и каким людям нужно особенно пристально следить за состоянием желудка.
Методы диагностики рака желудка
Важно не смешивать онкоскрининг с диагностикой в привычном понимании. Скрининг – это именно профилактическое обследование, первый и самый быстрый этап в постановке диагноза. Результат скринингового теста – не полная клиническая картина, а только первоначальное понимание: с органом все в порядке или возможны патологии, и нужно обследовать дальше.
В качестве методов быстрого обследования могут применяться:
1. Анализ крови на онкомаркеры – антигены и другие вещества, концентрация которых в крови меняется при онкологических заболеваниях. Недостаток такого анализа в его невысокой точности: даже положительный тест далеко не всегда свидетельствует о наличии злокачественных образований в желудке. Но пройти дополнительную диагностику при повышенном уровне онкомаркеров все же стоит обязательно.
2. УЗИ желудка или УЗИ брюшной полости – простая и комфортная для пациента процедура, которая дает необходимый минимум информации о состоянии желудка. Однако, по сравнению с эндоскопическим исследованием, этот метод гораздо менее точный.
3. Рентгенография желудка с контрастом. Перед процедурой в организм вводится контрастное вещество, которое способно накапливаться в тканях и делает полый орган отчетливо видимым на снимках. Недостаток метода – лучевая нагрузка на организм, поэтому без особых показаний такую диагностику не проводят.
4. При наличии жалоб – ФГДС, эндоскопическое исследование желудка и двенадцатиперстной кишки.
Если скрининговое исследование показало возможные проблемы с желудком, врач назначит дополнительную диагностику.
Скрининг рака желудка с помощью биосканера TRIMprob
Сканирование с помощью устройства TRIMprob – еще один метод ранней диагностики рака желудка, который недавно стал доступен пациентам клиники MedEx. В России он пока проходит апробацию и не распространен широко, но точность биосканера уже подтверждена на практике. Впервые инновация появилась в Италии, и сегодня такое оборудование используется в европейских клиниках для комфортного онкоскрининга.
Биосканер представляет собой датчик, который излучает безопасные для организма электромагнитные волны. По тому, как разные участки обследуемого органа поглощают сигналы, устройство может обнаружить патологии: воспаления, доброкачественные новообразования или раковые клетки. При выявлении проблем после сканирования врач направит на традиционную диагностику, а после можно будет планировать лечение.
В чем преимущества такого метода скрининга:
1. Быстрота – процедура длится недолго, а результат можно узнать практически сразу;
2. Точность – обследуется именно желудок, поэтому патологии в других органах не могут исказить результаты скрининга, как в случае с тестами на онкомаркеры;
3. Комфорт – исследование неинвазивное, датчик во время процедуры находится на расстоянии от кожного покрова;
4. Высокая чувствительность биосканера к патологиям даже на ранней стадии, которая доказана за годы использования этого прибора в Европе.
Кто находится в группе риска
Некоторые хронические болезни, вредные привычки и негативные факторы повышают риск злокачественных новообразований, и это важно иметь в виду для успешной диагностики рака желудка на ранней стадии.
К таким факторам относятся:
- ГЭРБ – гастроэзофагеальная рефлюксная болезнь, при которой содержимое желудка регулярно забрасывается в пищевод (ощущается, как частая изжога);
- Наследственная предрасположенность – если у ближайших родственников диагностировали рак желудка;
- Гастрит – длительное воспаление слизистой желудка;
- Полипы в полости желудка;
- Удаленный в прошлом желчный пузырь;
- Обилие пересоленой, копченой, консервированной пищи, жареной пищи;
- Недостаток фруктов и овощей в рационе;
- Курение;
- Лишний вес;
- Малоподвижный образ жизни;
- Инфекция Helicobacter Pylori, потенциально вызывающая различные патологии, – еще один фактор риска.
Процент заболеваемости у людей, подверженных этим факторам риска, по статистике, выше средних значений. Им необходимо обследоваться чаще и начинать делать это раньше. Оптимальным решением будет ежегодное плановое обследование, метод поможет подобрать ваш лечащий врач.
Показания для внепланового обследования: какие симптомы должны насторожить
Скрининговое обследование проводится даже тогда, когда симптомов нет, и человек считает себя здоровым. А при наличии жалоб тем более важно записаться к врачу и обследоваться.
Сигналом к внеплановому скрининговому исследованию служат:
- Тяжесть в желудке даже после небольшого количества съеденной пищи;
- Частая тошнота, для которой нет объективных причин;
- Боли в животе;
- Часто повторяющаяся рвота;
- Постоянная изжога;
- Частые расстройства пищеварения;
- Резкое снижение веса, общая усталость.
Большая часть этих симптомов указывают на воспалительный процесс в желудке и другие относительно неопасные патологии, но удостовериться в этом и выявить причину нужно обязательно.
Ранняя диагностика рака желудка в Москве
Регулярно оценивать состояние желудка особенно важно людям, которые находятся в группе риска или столкнулись с тревожными симптомами со стороны пищеварительной системы. Раннее выявление любых патологий повышает шансы вылечиться и продолжать жить полной жизнью.
В клинике MedEx вы можете пройти скрининг на рак желудка отдельно или в составе комплексной программы проверки здоровья. Подобрать подходящее решение вам поможет врач во время персональной консультации.
Источник
Исследование на онкомаркеры
Диагностировать рак желудка без применения сложных и не всегда легко переносимых исследований, к сожалению, пока невозможно. Хотя распространённой практикой «диспансеризации» уже стало исследование онкомаркеров. К сожалению, этот метод трудно отнести к высокочувствительным (чувствительность этих тестов не превышает 50%). И все же повышение значений СА 72-4, РЭА, СА 19-9 служит сигналом к обязательному углубленному обследованию и исследованию увеличенного показателя в динамике.
Большее значение онкомаркеры имеют при оценке распространенности процесса и при возникновении рецидива заболевания после успешного лечения.
Симптомы
Для ранних стадий рака желудка характерно обилие паранеопластических симптомов, часто маскирующих развитие опухоли и уводящих в сторону от правильного диагноза.
- Один из самых ярких симптомов — черный акантоз, при котором развивается сопровождающаяся ворсинчато-бородавчатыми разрастаниями темная пигментация кожи подмышечных впадин и других крупных кожных складок. Иногда черный акантоз на несколько лет опережает проявления самой опухоли.
- Полимиозит, дерматомиозит, кольцевидная эритема, пемфигоид, не уступающий лечению тяжелый себорейный кератоз также требуют углубленного обследования с обязательным проведением эндоскопии желудка.
- Бывают случаи, когда выработка клетками опухоли глюкокортикоидных гормонов, которые в норме синтезируются надпочечниками, вызывает даже формирование т.н. эктопического синдрома Кушинга. При нем жировая ткань откладывается преимущественно на лице и животе (так называемый матронизм), повышается артериальное давление, развивается склонность к переломам костей и акне.
- Частым паранеопластическим проявлением рака желудка, впрочем, как и многих других опухолей является мигрирующий тромбофлебит (синдром Труссо).
- Тяжелее всего заподозрить развитие рака желудка, когда у пожилых людей вдруг начинает быстро прогрессировать деменция, или появляются нарушение координации движений, изменение походки, нарушение равновесия.

Ситуация усугубляется сходством клинической, рентгенологической и эндоскопической картины при изъязвленных опухолях и язвенной болезни. Поэтому самым чувствительным способом диагностики считается эзофагогастродуоденоскопия (ЭГДС, гастроскопия) с множественной биопсией, обязательной у пациентов, относящихся к группе риска. ЭГДС позволяет одновременно:
- выполнить биопсию и провести дальнейшее гистологическое и цитологическое исследование с целью морфологической верификации новообразования и диагностики;
- осуществить лечебные манипуляции по коагуляции полипа с его удалением при небольших размерах (до 2 см);
- остановить кровотечение;
- провести зонд для кормления и т.д.
При угрозе кровотечения используется менее травмирующая браш-биопсия. В сомнительных случаях назначают повторную биопсию через 8-12 недель. Но даже этот способ диагностики дает правильный ответ только в 90% случаев и может дать ложно отрицательный результат при инфильтративном росте опухоли (такой рак называют скирр).
Кроме рака в желудке могут развиваться и опухоли из других клеток, требующие совершенно иных подходов к лечению (саркома, лимфома). Единственный способ разобраться в этом — множественные биопсии при проведении ЭГДС. Для выявления измененных участков тканей, не обнаруживаемых при обычном осмотре, используют т.н. хромогастроскопию. Этот метод позволяет проводить диагностику опухолей на ранних стадиях благодаря тому, что при окрашивании слизистой оболочки желудка по время процедуры специальными красителями (конго-рот/метиленовым синим, индигокамином) и даже раствором Люголя опухолевые ткани выглядят иначе, чем здоровые.
Когда необходимо проведение ЭГДС (гастроскопии)?
Существуют заболевания, считающиеся предраковыми, при которых необходимо периодическое обследование независимо от наличия симптомов. К ним относят:
- хронический атрофический гастрит с т.н. кишечной метаплазией особенно при наличии хеликобактерной инфекции;
- язвенная болезнь желудка;
- пищевод Баррета;
- дефицит витамина В12 (пернициозная анемия);
- аденоматозные полипы желудка;
- гипертрофическая гастропатия.
Операции на желудке в связи с доброкачественными новообразованиями, перенесенные более 10-лет назад, и отягощенная наследственность также относятся к ситуациям, требующим пристального наблюдения.
Вы должны регулярно наблюдаться с обязательным регулярным проведением ЭГДС, если у ваших родственников диагностировались:
- рак органов желудочно-кишечного тракта,
- семейный аденоматозный полипоз толстой кишки,
- синдром Гарднера,
- синдром Пейтца-Егерса,
- семейный ювенильный полипоз,
- синдром Ли Фраумени.
С развитием генетики стали известны некоторые гены, определенные мутации которых при особых условиях приводят к раку желудка.
Существуют и регионы, в которых, видимо в результате особенностей питания или экологии, заболеваемость существенно выше средних показателей (Япония, некоторые страны Европы, Скандинавия, Южная и Центральная Америка, Китай, Корея, страны бывшего СССР). Людям, длительно живущим в этих районах, надо внимательнее относиться к своему здоровью и периодически проводить ЭГДС. Сигналом к обязательному обследованию может послужить такой показатель как концентрация пепсиногена сыворотки крови (в норме — меньше 70 нг/мл) и соотношение его фракций (ПГ1/ПГ2).
При невозможности проведения ЭГДС, например, из-за сопутствующих заболеваний, может быть проведена полипозиционная рентгенография с двойным контрастированием бариевой взвесью и воздухом. Этот метод обладает, правда, гораздо меньшей чувствительностью при ранних стадиях заболевания и не дает возможности морфологической верификации. Дополнительно используют МСКТ и УЗИ, однако точность последнего исследования даже при опытном исследователе очень зависит от технических возможностей аппарата, особенностей телосложения и правильности подготовки пациента.
Лапароскопическая диагностика желудка
При подозрении на распространение опухоли по брюшной полости возможно проведение диагностической лапароскопии и лапароскопического УЗИ, позволяющих подробно изучить процесс в непосредственной близости.
Этот метод позволяет осмотреть поверхности печени, передней стенки желудка, париетальной (выстилающей стенки брюшной полости) и висцеральной (покрывающей органы) брюшины с проведением при необходимости биопсии. В некоторых случаях эти данные принципиально важны для выбора лечения.

Прогноз при раке желудка
Прогноз зависит от количества пораженных лимфатических узлов и уровня поражения лимфатических коллекторов, глубины прорастания опухоли в стенку желудка, стадии процесса, типа роста и типа самой опухоли. По данным МНИОИ им. П.А.Герцена 5-летняя выживаемость при диагностике рака желудка на ранней стадии и быстро начатом лечении достигает 85-90%. В случае более позднего выявления ещё резектабельной опухоли — 11-54%, и даже в случае выявления рака на IV стадии лечение позволяет обеспечить 7% выживаемость больных в течение 5 лет.
Цены в Европейской клинике на диагностику рака желудка
- ЭДГС высокой четкости с цифровой записью, диагностическая — от 14300 руб.
- Рентгеноконтрастное исследование пищевода и желудка — 20700 руб.
- Ультразвуковое исследование брюшной полости (печень, желчный пузырь, желчные протоки, селезенка, поджелудочная железа), в т. ч. с определением уровня свободной жидкости — 7000 руб.
- Диагностическая лапароскопия — 57500 руб.
Но речь ведь не только о продлении жизни. Цель лечения в большинстве даже далеко зашедших случаев в улучшении её качества, избавлении человека от множества тягостных симптомов, в том числе болей, обеспечении ему возможности вести обычный образ жизни, заниматься важными для него делами, общаться с близкими.
Современные методы лечения рака желудка, применяемые в Европейской клинике, позволяют проводить лечение с минимальными сроками госпитализации и использованием малоинвазивных методик, улучшающих не только прогноз для жизни, но и качество самой жизни наших пациентов.
Источник
Рак пищевода представляет собой опухоль злокачественного характера, происходящую из эпителиальных клеток пищевода. Заболевание берет начало с внутреннего слоя, то есть слизистой оболочки, а затем распространяется наружу, преодолевая подслизистый и мышечный слои.
Существует два основных вида такого заболевания:
- Плоскоклеточный рак. Он возникает из клеток, составляющих слизистую оболочку пищевода. Чаще всего встречается в зоне шеи, а также двух верхних третей грудной клетки.
- Аденокарцинома, другими словами – железистый рак. Чаще всего диагностируется в нижней трети пищевода. Вначале происходит замещение железистого эпителия плоскоклеточным (при пищеводе Барретта).
Статистика
Это одно из самых агрессивных злокачественных заболеваний. Рак пищевода занимает 8-е место по смертности во всем мире. В соответствии с данными Международного агентства по изучению рака, в 2018 году заболеваемость – 7,49 случая на 100 000 человек в год, а смертность – 6,62. Расчеты же Росстата Минздрава России говорят, что заболеваемость составляет 5,6 случая на 100 000 человек. Среди мужчин – 9,43 на 100 000, среди женщин – 2,29 на 100 000.
Наиболее часто заболевание диагностируется в так называемом «азиатском поясе», то есть от северной части Ирана, через Среднюю Азию и до центральных регионов Японии и Китая, также захватывая Сибирь. Во много это объясняется особенностями рациона людей, проживающих в этих районах.
Чаще всего (до 80% случаев) новообразование находится в нижне- и среднегрудном отделах пищевода. С частотой 10-15% случаев диагностируется рак шейного отдела пищевода.
Факторы риска
Основные факторы риска возникновения и развития такой болезни:
- мужской пол, потому что мужчины чаще подвержены вредным привычкам – курению и употреблению спиртного в больших количествах;
- возраст – чем он больше, тем выше риск, лишь 15% пациентов были младше 55-ти лет;
- избыточная масса тела;
- курение и злоупотребление спиртным;
- употребление очень горячих напитков и еды;
- пищевод Барретта (когда в нижней части пищевода возникает клеточное перерождение, вызываемое кислотным повреждением хронической формы);
- рефлюкс;
- ахалазия (когда нарушена запирательная функция отверстия между желудком и пищеводом);
- рубцы в пищеводе, приведшие к его сужению;
- синдром Пламмера-Винсона (для такого синдрома характерна триада, то есть три вида нарушений одновременно: нарушенная глотательная функция, суженный пищевод, железодефицитная анемия);
- контакт с химикатами.
Примерно у 1/3 заболевших диагностирован ВПЧ (вирус папилломы человека).
Риск заболеть этим видом рака можно снизить, если разнообразно питаться, не пить крепкий алкоголь, а при наличии синдрома Барретта отслеживать изменения в слизистой оболочке.
Скрининг этого заболевания не проводится. Однако при повышенном риске появления рака пищевода рекомендуется проходить эндоскопическое исследование, при необходимости с биопсией подозрительной зоны.
Симптомы
Обычно рак пищевода обнаруживается на поздних стадиях, когда терапия уже осложнена, или случайно.
Наиболее частая симптоматика включает следующее:
- Дисфагия. Этот симптом представляет собой нарушенную функцию глотания. Пациенты описывают свое состояние как ощущение «комка в горле». Заболевшие начинают уменьшать порции пищи, избегают твердой еды. На поздних стадиях возможно употребление только жидкой пищи.
- Повышенное слюноотделение. Больше слюны в ротовой полости начинает вырабатываться для того, чтобы помочь продвинуться пищевому комку через суженный просвет пищевода.
- Дискомфорт и боль в грудине. Эти симптомы не всегда относятся к раку пищевода, они могут вызываться межреберной невралгией, стенокардией, гастроэзофагеальным рефлюксом. Поэтому не являются специфическими.
- Снижение массы тела. При затрудненном глотании и общей слабости заболевший человек начинает отказываться от еды, поэтому похудение часто сопровождает рак пищевода.
Есть и более редкие симптомы:
- кашель;
- икота;
- хриплый голос;
- рвота;
- костные боли (при наличии метастазов);
- пищеводное кровотечение (после того как кровь проходит по ЖКТ, стул окрашивается в черный цвет);
- как следствие кровотечения – анемия (человек становится бледным, слабым, быстро утомляется, испытывает постоянную сонливость).
Важно! Наличие подобных симптомов еще не означает рак. Однако нужно обязательно обратиться к врачу и обследоваться.
Классификация рака пищевода
По области возникновения:
- внутригрудной отдел пищевода;
- шейный отдел (от нижней границы перстневидного хряща до входа в грудную полость);
- верхняя грудная зона (от входа в грудную полость до области бифуркации трахеи);
- средняя грудная область (проксимальная часть пищевода распространяется от зоны бифуркации трахеи до соединения пищевода с желудком);
- нижняя грудная область (дистальная часть пищевода примерно 10 см в длине, включая абдоминальную часть пищевода, распространяется от зоны бифуркации трахеи до соединения пищевода и желудка).
По характеру роста опухоли:
- в просвет пищевода (экзофитный);
- язвенный (эндофитный);
- круговая форма (инфильтративный склерозирующий).
По степени дифференцировки новообразования:
- степень не определена – Gx;
- высокодифференцированное образование – G1;
- умеренно дифференцированное – G2;
- малодифференцированное – G3;
- недифференцируемое – G4.

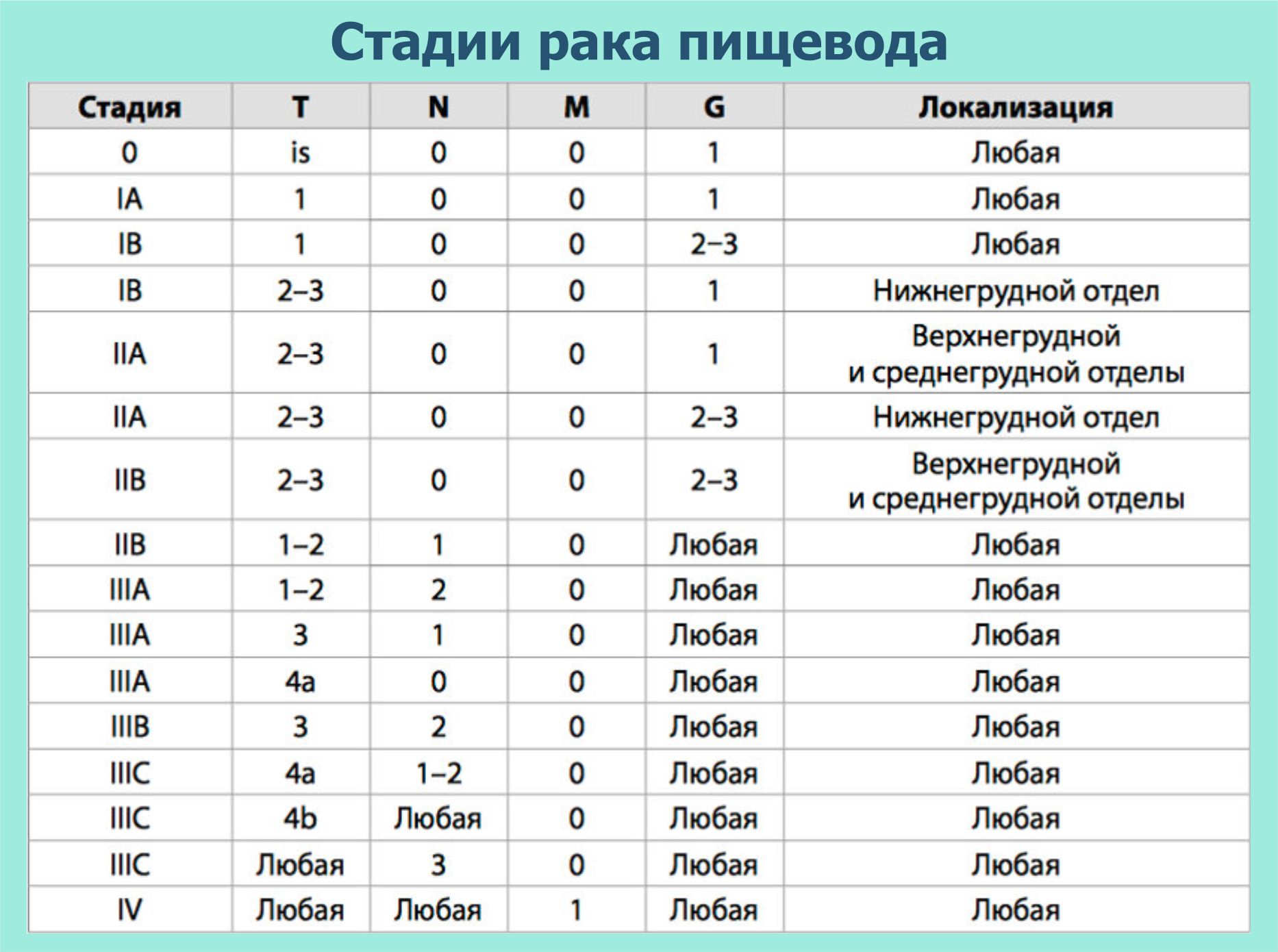
Стадии рака пищевода
Предлагаем ознакомиться с таблицей стадирования заболевания:
Диагностика
Диагностирование осуществляется инструментальными и лабораторными методами.
- Рентгенография с бариевым контрастом. Пациент принимает внутрь сульфат бария, который обволакивает стенки пищевода. Это позволяет увидеть на снимке рельеф стенок и обнаружить сужение просвета. На ранней стадии рак может иметь вид небольших круглых выпуклостей, то есть бляшек. На поздней стадии развития новообразование принимает вид большой опухоли неправильной формы, которая может вызывать сильное сужение пищевода. Рентгенография также позволяет диагностировать трахеопищеводную фистулу, то есть когда из-за разрушения новообразованием стенки пищевода на всю толщину пищевод начинает сообщаться с трахеей.
- КТ (компьютерная томография). Это исследование дает возможность визуализировать то, насколько процесс распространился на находящиеся рядом органы, определить наличие отдаленных метастазов и поражение лимфоузлов.
- МРТ (магнитно-резонансная томография). С ее помощью выявляют очаги поражения спинного и головного мозга. Преимущество исследования – отсутствие лучевой нагрузки на пациента. В последнее время проводится МРТ пищевода, данная методика новая , но уже хорошо зарекомендовала себя.
- ПЭТ (позитронно-эмиссионная томография) и ПЭТ-КТ (ПЭТ, совмещенная с компьютерной томографией). «Подсвечивают» все очаги онкологии в организме и определяют уровень активности в них. Применяются, чтобы выявить отдаленные метастазы и поражение лимфоузлов. ПЭТ-КТ дает возможность соотнести те области, где тканями, в которых содержатся быстро делящиеся клетки, накопилось радиоактивное вещество, со снимками на КТ.
- Обследование эндоскопическим методом. Дает возможность установить причину, по которой нарушена функция глотания, увидеть размер и распространенность новообразования, сделать биопсию подозрительной области.
- Эндо-УЗИ, то есть применение эндоскопа с ультразвуковым датчиком. При таком обследовании можно точно определить, на какую глубину опухоль проросла в стенку пищевода, вовлечены ли соседние ткани, включая лимфоузлы, а также сделать биопсию.
- Бронхоскопия. Позволяет оценить состояние трахеи, если есть вероятность, что новообразование распространилось на ее стенку.
- Торакоскопия. В ходе такого обследования оценивают состояние органов грудной полости и лимфоузлов.
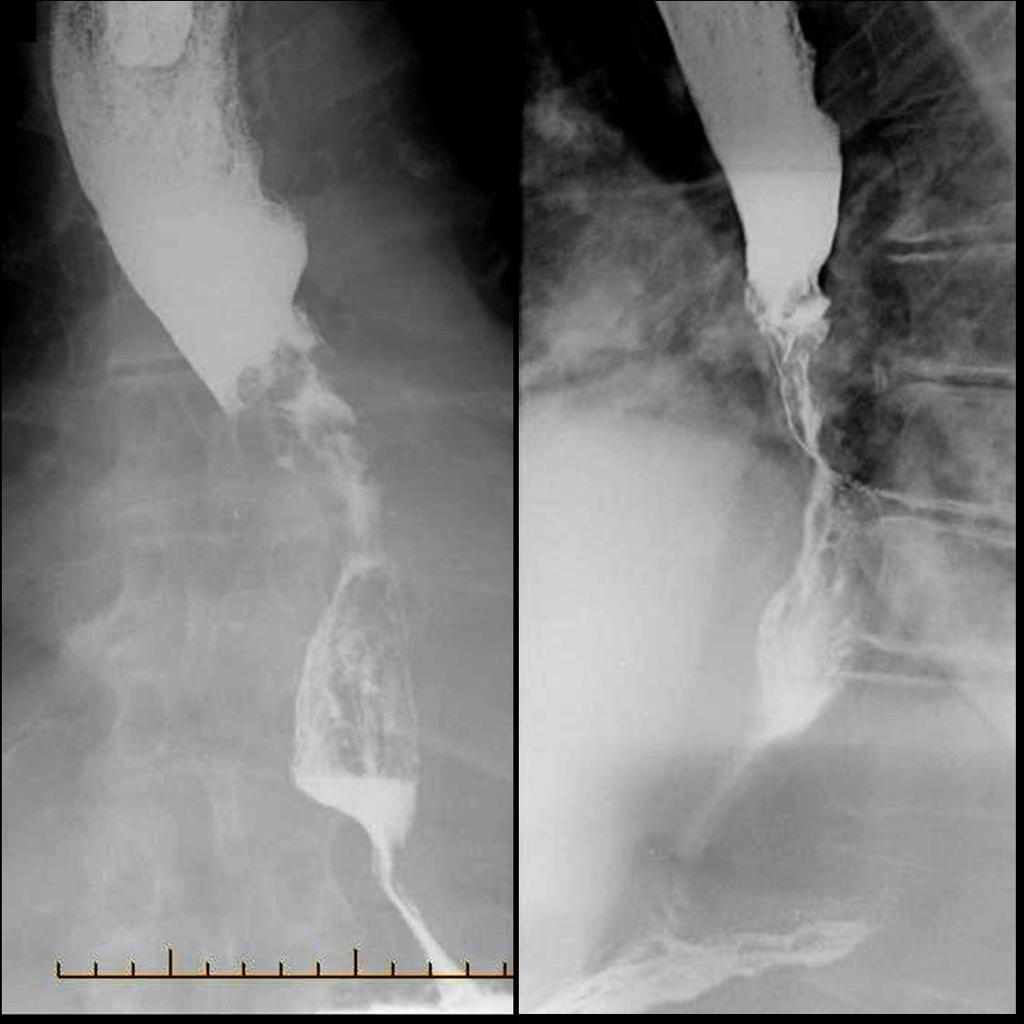
Рентгенодиагностика рака пищевода
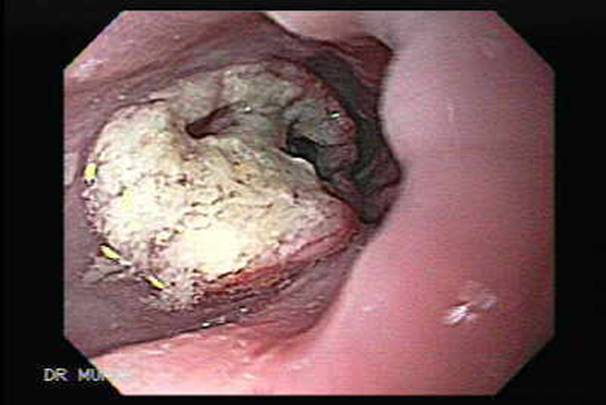
Эндоскопическая картина плоскоклеточного рака
Лабораторные исследования
- Клинический анализ крови. Позволяет выявить анемию, которая возникает из-за кровотечения или скудного рациона.
- Биохимический анализ крови. Он показывает состояние внутренних органов, а именно почек, печени и др.
- Анализ на онкомаркеры СА 19-9, РЭА.
- Исследование биоматериала, взятого во время биопсии. В нем определяют рецепторы белка HER2. При их наличии против новообразования можно использовать таргетную терапию.
Лечение
Основной метод лечения – хирургическая операция, однако комплексный подход позволяет улучшить результаты. Поэтому различные методики комбинируются.
Хирургическое лечение
В ходе операции удаляют пищевод целиком или его часть, все зависит от распространенности и локализации патологического процесса.
Когда опухоль находится в шейном отделе, удаляют большую часть пищевода. После этого желудок поднимают и подшивают к оставшейся части пищевода. Кроме того, вместо удаленной части методом пластической операции может быть использована часть толстой или тонкой кишки. При возможности выполнения резекции шейного отдела пищевода может быть выполнена пластика кишкой с микрососудистым анастомозом сосудов на шее.
При локализации опухоли в шейном отделе пищевода с большим распространением приходится выполнять операцию в объеме: удаления фаринголарингоэктомии с одномоментной пластикой пищевода желудочным трансплантатом, с пришиванием его к корню языка.
Хирургическое вмешательство по удалению части пищевода с последующим замещением трансплантатом может быть проведено открытым способом или методом торакоскопии и лапароскопии.
При любом типе вмешательства удаляют регионарные лимфоузлы, которые потом исследуют в лаборатории методом гистологии. Если в них обнаруживаются раковые клетки, то после операции пациенту прописывают лучевое лечение или химиотерапию в комбинации с ЛТ.
Также существуют паллиативные операции. Их проводят для того, чтобы пациент мог питаться, если из-за опухоли он не может глотать. Этот тип вмешательства называется гастростома, то есть введение через переднюю брюшную стенку в желудок специальной трубки для питания.
Лучевая терапия
Применяется ионизирующее излучение с целью уничтожения клеток новообразования. Такая терапия может проводиться:
- Тем пациентам, которым по состоянию здоровья нельзя делать операцию. В этом случае облучение, обычно вместе с химиотерапией, представляет собой основную методику лечения.
- При локализации опухоли в области шейного отдела пищевода химиолучевая терапия является первым этапом комбинированного метода лечения.
- Перед операцией вместе с химиотерапией. Это нужно, чтобы уменьшить опухоль и обеспечить ее лучшее удаление (называется «неоадъювантная терапия»).
- После хирургического вмешательства вместе с химиотерапией. Таким образом воздействуют на остаточную опухоль, которую нельзя было увидеть во время операции (носит название «адъювантная терапия»).
- Для облегчения симптоматики при распространенном раке пищевода. Позволяет снизить интенсивность болевого синдрома, устранить кровотечение и трудности с глотанием. В данном случае это паллиативная терапия.
Разновидности лучевого лечения:
- Наружное (дистанционное). Источник ионизирующего излучения находится на расстоянии от пациента.
- Контактное (называется «брахитерапия»). Источник излучения эндоскопическим методом размещается как можно ближе к новообразованию. Ионизирующие лучи проходят малое расстояние, поэтому достигают опухоли, но мало затрагивают расположенные рядом ткани. Лечение позволяет уменьшить новообразование и восстановить проходимость.
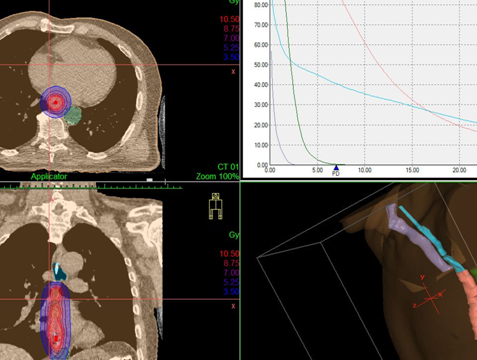
Дозное распределение, получаемое при дистанционной конформной лучевой терапии и внутрипросветной брахитерапии
Химиотерапия
Данная методика представляет собой введение в организм препаратов, затормаживающих жизнедеятельность опухолевых клеток или уничтожающих их. Лекарственные средства принимаются внутрь или вводятся в вену, после чего попадают в кровоток и достигают почти всех областей организма.
Химиотерапия осуществляется циклами. Это связано с тем, что действие препарата направлено на те клетки, которые постоянно делятся. Введение повторяется через определенное число дней, что связано с клеточным циклом. Циклы химиотерапии, как правило, имеют продолжительность 2-4 недели, больным обычно показано несколько циклов.
Как и облучение, химиотерапия показана в адъювантном и неоадъвантном режимах. Также она применяется, чтобы облегчить симптоматику тем больным, у которых рак распространен и не поддается хирургическому лечению.
Некоторые препараты:
- «Цисплатин» и «5-фторурацил» («5-FU»);
- «Паклитаксел» и «Карбоплатин»;
- «Цисплатин» совместно с «Капецитабином»;
- схема ECF: «Эпирубицин», «Цисплатин» и «5-FU»;
- схема DCF: «Доцетаксел», «Цисплатин» и «5-FU»;
- «Оксалиплатин» совместно либо с «Капецитабином», либо с «5-FU»;
- «Иринотекан».
Таргетная терапия
Направлена на блокировку роста новообразования путем воздействия на определенные мишени, то есть на те молекулы, которыми определяются деление и рост опухоли. Если в биоматериале, взятом методом биопсии, находят такие белковые молекулы, то может быть эффективна именно таргетная терапия.
Паллиативные методы
При проведении паллиативной терапии применяют следующие методики:
- Бужирование, то есть расширение пищевода.
- Установку стентов эндоскопическим методом. Стенты – это полые цилиндры, которые устанавливаются в просвет пищевода, чтобы обеспечить проходимость пищи.
- Лазерную фотокоагуляцию (новообразование разрушают лазером).
- Фотодинамическое воздействие. Пациенту вводится фотосенсибилизатор, который накапливается клетками опухоли. Затем под действием лазерного луча с определенной длиной волны эти клетки погибают.
- Химиотерапия и облучение. Могут применяться, чтобы уменьшить размер новообразования и восстановить проходимость.
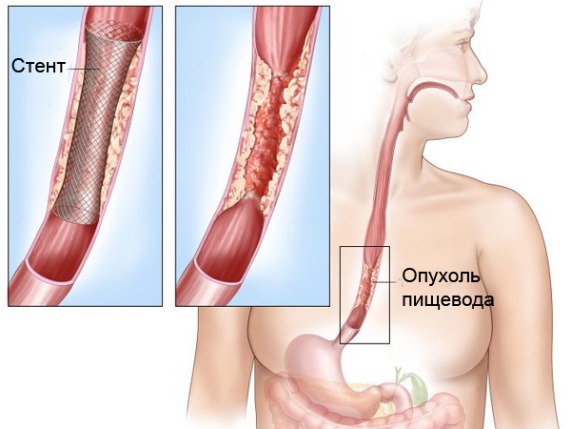
Стентирование рака пищевода