У собаки дискинезия желчного пузыря

Пароксизмальная дискинезия (ПД) – это полиэтиологическое неврологическое заболевание, которое проявляется эпизодическими двигательными нарушениями с различной клинической картиной и характеризуется внезапными атаками патологической непроизвольной двигательной активности в различных группах мышц, протекающими при сохранении сознания.
К большому сожалению, несмотря на некую популярность данной патологии в последнее время, в клинической ветеринарной практике гиперкинетические расстройства все же изучены плохо. В настоящее время отсутствуют специфические диагностические методы, позволяющие диагностировать пароксизмальные дискинезии. Одними из ключевых причин, при которых дискинезии остаются недодиагностированными, являются неоднородность клинических проявлений и этиологии, возможность одновременного существования сразу нескольких типов мышечных атак. По мнению Clare Rusbridge, дискинезии могут одновременно протекать с самой эпилепсией, однако в настоящий момент не существует достаточной доказательной базы и соответствующих исследований относительно этого утверждения.
Принципиальное значение имеет этиологическая классификация дискинезий, согласно которой выделяют первичную или наследственную дискинезию и приобретенную (вторичную, симптоматическую) дискинезию, развивающуюся как следствие приобретенных эндо- и экзогенных патологических состояний.
На основании молекулярно-генетических исследований получены данные и выделено несколько десятков мутаций, ассоциированных с развитием первичных дискинезий, однако точные патофизиологические механизмы возникновения данных мутаций до сих пор не изучены. Имеются веские доказательства, что для клинического проявления дискинезии необходима дисфункция базальных ядер различной тяжести, сопровождающихся повышением активности дофаминергических структур при неизмененном уровне самого дофамина.
Базальные ядра – это несколько скоплений серого вещества, расположенных в белом веществе на уровне основания полушарий. Данные структуры обеспечивают функциональную регуляцию движений, формируя стриопаллидарную систему (рис. 1).
Черная субстанция играет важную роль в регуляции моторной функции и тонуса мышц, в ней синтезируется дофамин, без которого не может быть начато движение. Взаимодействие черной субстанции и стриопаллидарной системы основано на прямых и обратных связях между ними, поэтому при поражении системы развивается дискинезия – нарушение двигательных актов (рис. 2).
Иными словами, в патогенезе дискинезии важную роль играют нарушения центральной регуляции мышечного тонуса, в результате которых изменяется механизм иннервации и возникает патологический «спазм антагонистов», что приводит к развитию своеобразных гиперкинезов и позных нарушений (рис. 3).
Dennis O’Brien
Симптоматическая (приобретенная) дискинезия часто связана с повреждениями головного мозга в области базальных ядер и ядер таламуса.
Вторичная форма дискинезий может проявляться при различных заболеваниях, которые опосредованно влияют на механизм центральной регуляции, ими могут быть инфекционные заболевания, метаболические нарушения, интоксикации, в том числе на фоне лекарственной терапии.
При применении препарата метоклопрамид (церукал) следует учитывать риск возникновения гиперкинетического синдрома у животных, так как установлена возможность экстрапирамидных расстройств на фоне его использования.
До сих пор также не создано унифицированной классификации дискинезий. В качестве классификационных критериев могут быть использованы как типы мышечных атак, так и провоцирующие факторы (кинезиогенные – некинезиогенные) и прочие.
По типу мышечных гиперкинетических атак пароксизмальные дискинезии подразделяются на дистонию, хорею и реже встречающиеся в ветеринарной практике атетоз и баллизм.
Дистония – это длительное сокращение мышц тазовых конечностей, проявляющееся как усиленный тонус разгибателей. Может приводить к скручиванию (торсиям), часто повторяющимся движениям и позам.
Данные мышечные атаки имеют особенность в виде их постоянной направленности, т.е. дистонические движения следуют определенному образцу и постоянно охватывают одни и те же мышечные группы у одного индивида. В процессе дистонической атаки могут вовлекаться определенные группы мышц черепа, приводя к развитию гемифациального гиперкинеза (рис. 4).
Хорея (хореический гиперкинез) – нерегулярные, отрывистые, беспорядочные, хаотичные, иногда размашистые, бесцельные движения, возникающие преимущественно в конечностях. Выраженный хореический гиперкинез напоминает движения «чертика на ниточке» и искажает стояние и ходьбу, приводя к странной, вычурной, «клоунской» походке, которая плохо поддается адекватному описанию. Животные при хореическом гиперкинезе не могут передвигаться из-за падений.
По провоцирующим факторам пароксизмальные дискинезии в гуманной медицине ранее подразделялись на 4 формы. К ним относились пароксизмальная кинезиогенная дискинезия, пароксизмальная некинезиогенная дискинезия, пароксизмальная дискинезия, индуцированная физической нагрузкой, и пароксизмальная гипногенная дискинезия. Четвертая форма пароксизмальной дискинезии, описанная как «гипногенная пароксизмальная дискинезия» (Bhatia K. P., 2001), предполагала эпизоды дискинезий, возникающих только во время сна. Впоследствии была доказана эпилептическая сущность этого состояния как одной из форм ночной лобной эпилепсии, поэтому гипногенная пароксизмальная дискинезия была исключена из классификаций дискинезий.
Пароксизмальная кинезиогенная дискинезия проявляется частыми и короткими эпизодами (в большинстве случаев меньше одной минуты) насильственных движений, с одной из отличительных черт данной патологии – провокацией эпизодов движением. Испуг и вздрагивание также могут провоцировать атаку. В моторном рисунке эпизода доминируют тонические и дистонические, реже другие движения и позы. Важным является то, что данные эпизоды с успехом контролируются антиконвульсантами.
Пароксизмальная некинезиогенная дискинезия проявляется непровоцируемыми эпизодами гиперкинезов, которые происходят спонтанно в состоянии покоя. Так же как и при любых формах дискинезий, неврологический статус между атаками в норме.
Пароксизмальная дискинезия, обусловленная физической нагрузкой, занимает среднее положение между кинезиогенной и некинезиогенной дискинезией и проявляется двигательными гиперкинезами после длительной или чрезмерной физической нагрузки. Ведущим гиперкинезом при данном типе дискинезии является дистонический тип мышечной атаки.
В клинической ветеринарной практике значительные трудности представляет диагностика моторных приступов эпилептической и неэпилептической природы. Ветеринарный врач всегда находится в трудном положении при выборе терапии в условиях отсутствия видеозаписи эпизода и грамотного словесного его описания владельцем. Неправильная интерпретация данных анамнеза неизбежно приводит к ошибочной диагностике эпилепсии в большом количестве случаев. Диагностика пациентов с моторными нарушениями строится, как правило, на комплексе клинических и параклинических методов, включающих биохимические, генетические, нейровизуальные и нейрофизиологические методы, оценку электролитных нарушений, а также оценку титра на глиадин и тканевую трансглютаминазу. Важно не забывать о сборе анамнеза с учетом породных часто встречающихся болезней и регистрации видеозаписи эпизода.
Визуально отличить уровень сознания у собак очень сложно. Дифференцировать фокальные, простые очаговые и тонические приступы эпилепсии можно на основании данных ЭЭГ, а именно при наличии на ней спайк-волны. Однако при записи неинвазивной ЭЭГ, т.е. без имплантированных на длительное время электродов, оценка спайк-волны включает большое количество артефактов из-за мышечной нагрузки во время эпизода. Также немаловажен тот факт, что эпизоды могут быть довольно редкими, это делает весьма проблематичным длительную запись электрической активности головного мозга без ЭЭГ Холтера.
Магнитно-резонансная томография необходима для оценки структурных изменений головного мозга. У пациентов с первичной пароксизмальной дискинезией на МРТ не выявляются структурные изменения головного мозга в области базальных ядер.
Синдром эпизодического падения у кавалер-кинг-чарльз-спаниелей на сегодняшний момент доступен для диагностики в России с помощью генетического анализа буккального соскоба.
Существует немногочисленное исследование собак в рамках породы бордер терьер, в пределах одной кровной линии, имеющих клинические признаки пароксизмальной некинезиогенной дискинезии. Данное исследование содержит в своих выводах некую доказательную базу о влиянии на двигательные нарушения глютена. В крови у собак этой группы были выявлены высокие титры к глиадину и тканевой трансглютаминазе, и при назначении специфической безглютеновой диеты клинические проявления уходили, что дало повод предполагать о наличии такой связи, а именно: проявлений мышечных атак и глютена. Однако подобных исследований собак других пород не проводилось.
Торсионные движения и позы могут быть вызваны различными нарушениями центральной и периферической нервной системы, а также нарушениями, не связанными с ней, так как далеко не все непроизвольные мышечные сокращения являются дискинезиями по своей природе. Поэтому для клинициста очень важно понять, с какой патологией он сталкивается при отсутствии специфических диагностических методов.
Дифференциальная диагностика
Дифференциальная диагностика судорожных приступов от атак гиперкинезов достаточно сложна и неоднозначна. Наиболее важным является то, что дискинезии всегда происходят без нарушения сознания, судороги же протекают с измененным сознанием, однако оценить уровень сознания у собак сложно.
Следует помнить, что и в гуманной медицине, и в ветеринарии не все судороги происходят с потерей сознания, хотя считается, что это ключевой диагностический признак. Есть так называемые простые очаговые приступы, при которых патологический электрический импульс возникает в части лобной доли головного мозга. Для проявления таких приступов, как правило, характерно участие мимических мышц или одной группы мышц (например, только одной конечности), и проходят они в сознании. Электроэнцефалография при лобной эпилепсии (по данным гуманной медицины) не регистрирует спайк-волны.
Двигательные пароксизмы могут быть индуцированы нагрузкой, стрессом или движением, что маловероятно для судорог, однако не следует забывать о некоторых типах эпилепсии, вызываемых резким шумом, светом и иным внешним раздражителем.
Для гиперкинезов также не характерна ни аура, ни постиктальный период, включающий дезориентацию, вокализацию, слепоту, жажду, голод, агрессию, беспокойство и прочее, равно как и генерализация в тонико-клонический припадок.
Дистонические проявления не сопровождаются автономными симптомами, такими как слюнотечение, дефекация, мочеиспускание. Однако при длительных гиперкинетических атаках, продолжающихся более часа, может возникать феномен гипервозбудимости автономной системы, проявляющийся рвотой, диареей и гипертермией.
Проявление мышечной слабости всегда говорит не в пользу дискинезии. По продолжительности судорожные приступы, как правило, не превышают 5–7 минут, за исключением статуса, некинезиогенные дискинезии могут продолжаться по несколько часов.
Нерегулярность чередования – один из ключевых признаков пароксизмальной дискинезии. У большинства собак эпизоды повторяются еженедельно или ежедневно, но частота может варьироваться от одного до нескольких десятков за сутки. Нередко отмечается волнообразное течение с выраженными колебаниями частоты и интенсивности атак.
Лечение
Так как дискинезии являются каналопатиями, лечение подобрать сложно. Каналопатии – это группа заболеваний, обусловленных мутациями генов ионных каналов. Поперечно-полосатая мышца относится к возбудимым тканям, нормальное функционирование которых определяется в первую очередь взаимодействием трансмембранных ионных потоков и состоянием ионных каналов. При дискинезиях нарушаются инактивации (закрытия) натриевого канала, в результате чего имеет место патологическая утечка натриевого тока в клетку и генерация потенциала действия.
Следует отметить, что контролируемых исследований эффективности препаратов, используемых для лечения пароксизмальной дискинезии, не проводилось. Лекарственная терапия в каждом случае подбирается, к сожалению, эмпирически.
Антиконвульсанты имеют переменный эффект и используются только в случае пароксизмальной кинезиогенной дискинезии. По сути, могут быть применены фенобарбитал, леветирацетам, пексион в рекомендованных при судорожных приступах дозировках, однако растет количество публикаций, в которых эффективность от применения данных препаратов отмечается как сомнительная. Наилучшим лекарственным средством в данной категории является антиконвульсант зонисамид (зонегран), механизм действия которого – инактивация натриевых каналов. В этой же связи также может быть упомянут габапентин, однако в настоящее время нет публикаций, касающихся его эффективности при лечении пароксизмальной дискинезии у собак.
Диакарб (ацетазоламид) назначают в дозе 5 мг/кг (Dennis O’Brien дает большую границу в 4–10 мг/кг). Клинический эффект диакарба в этих случаях связывают с блокадой карбоангидразы в нервных клетках и снижением их возбудимости. Однако на фоне применения ацетазоламида могут наблюдаться побочные проявления в виде заторможенности, метаболического ацидоза и гипокалиемии.
Ингибиторы карбоангидразы угнетают канальцевую реабсорбцию бикарбоната. Профилактика подобных проявлений должна заключаться в даче препаратов калия.
Диазепам перорально – в дозе 0,5 мг/кг 2 раза в день.
Ацепромазин (ветранквил) – 0,1–0,7 мг/кг, по данным различных источников. Ингибиторы серотонина – флуоксетин – 0,4 мг/кг.
Леводопа/бенсеразид – от 5 до 15 мг/кг 2 раза в сутки могут быть эффективны. Используется при снижении дофамина (описано у китайских хохлатых и керри-блю-терьеров клинически при неспособности начать произвольные движения). Препарат индуцирует рвоту. Необходимо начинать с наименьшей дозы, постепенно увеличивая дозировку.
Пациенты, показывающие высокий титр к глиадину и к тканевой трансглютаминазе в крови, должны получать безглютеновую диету.
Оценка эффективности проводимой терапии должна заключаться в уменьшении частоты и силы двигательных пароксизмов.
Менее чем у половины пациентов удается добиться ремиссии при приеме лекарственных средств, остальная часть сохраняет двигательные эпизоды всю жизнь. Небольшая доля эутаназируется по причине частых, неконтролируемых эпизодов мышечной атаки, причиняющих существенные эмоциональные и физические страдания как пациента, так и владельца. Отдельным пунктом можно рассматривать лабрадоров – их состояние способно улучшаться с течением времени без какой бы то ни было медикаментозной коррекции.
Заключение
За последние годы исследователи немного продвинулись в изучении генетических, патофизиологических механизмов возникновения первичных форм синдрома «пароксизмальные дискинезии», описываются и новые клинические варианты наследственных пароксизмальных неэпилептических расстройств движения у животных. Не исключено, что симптоматические пароксизмальные дискинезии также генетически детерминированы, а факторы внешней среды являются лишь пусковым механизмом реализации генетического дефекта.
Литература:
- Dennis O`Brien. Diagnosis & Treatment of Movement Disorders, 2016.
- Angelika Richter, Melanie Hamann, Jörg Wissel, Holger A. Volk. Dystonia and Paroxysmal Dyskinesias: Under-Recognized Movement Disorders in Domestic Animals? A Comparison with Human Dystonia/Paroxysmal Dyskinesias, 2014.
- Залялова З. А. Пароксизмальные дискинезии, доклад секция 2, 2015.
- Albanese A., Asmus F., Bhatia K. P. EFNS guidelines on diagnosis and treatment of primary dystonias. Eur J Neurol, 2011; 18: 5–18.
- Andrews C., Aviles-Olmos I., Hariz M., Foltynie T. Which patients with dystonia benefit from deep brain stimulation? A metaregression of individual patient outcomes. J. Neurol. Neurosurg. Psychiatry, 2010; 81: 1383–1389.
- Clare Rusbridge. Эпилепсия у собак и кошек, разбор сложных случаев, материалы неврологической конференции – СПб, 2015.
Источник
Д.Е. Митрушкин. Ветеринарная клиника «Биоконтроль», Клиника экспериментальной терапии ГУ РОНЦ им. Н.Н. Блохина РАМН
Ключевые слова: желчь, желчные камни, желчнокаменная болезнь, желчный проток, холелитиаз, желчный пузырь, холецистолитиаз, печень, печёночные протоки
Сокращения: АЛТ – аланинаминотрансфераза, КТ – компьютерная томография, РМЖ – рак молочной железы, УЗИ – ультразвуковое исследование, ЩВ – щелочная фосфатаза, ЭКГ – электрокардиограмма
Введение
Желчь – секрет, постоянно вырабатывающийся в печени и поступающий во внутрипечёночные желчные протоки, которые, сливаясь, формируют правый и левый внепечёночные протоки, расположенные вблизи ворот печени. Эти протоки соединяются и образуют общий печёночный проток, переходящий в общий желчный проток, впадающий в двенадцатиперстную кишку. Желчь поступает в желчный пузырь (резервуар для хранения желчи) из общего желчного протока через пузырный проток и из него же, по мере необходимости, выбрасывается обратно в общий желчный проток.
Желчнокаменная болезнь (холелитиаз, от греч. chole — жёлчь и lithos — камень) – обменное заболевание гепатобилиарной системы, характеризующееся образованием желчных камней в желчном пузыре (холецистолитиаз), реже – во внутрипечёночных желчных протоках (печёночный холелитиаз) или общем желчном протоке (холедохолитиаз).
Холелитиаз является редким заболеванием у собак и кошек. Даже его наличие у животных часто протекает бессимптомно и до введения УЗИ в ветеринарную практику чаще выявлялось лишь при аутопсии. Основной причиной образования желчных камней является нарушение функционального состояния печени (вследствие гепатитов, гепатозов или циррозов) и изменение в связи с этим физико-химических свойств желчи (дисхолия). Образование желчных камней связано с нарушением метаболизма основных составляющих желчи – холестерина, фосфолипидов (лецитина и др.), желчных кислот, желчных пигментов (билирубина, биливердина) и неорганических солей. Холестерин в составе желчи у здоровых животных благодаря холестеринудерживающим факторам (желчным кислотам и фосфолипидам) сохраняется в растворённом состоянии. При вышеуказанных патологиях печени количество этих двух холестеринудерживающих факторов падает ниже критического уровня и создаются благоприятные условия для образования коллоидных растворов холестерина с образованием густой неоднородной желчи (начальная или предкаменная стадия желчнокаменной болезни) с дальнейшей кристаллизации холестерина и формирования камней. Образование этих конкрементов может быть связано также с усиленной секрецией холестерина.
К предрасполагающим факторам желчнокаменной болезни относят наличие патологии (стеноз, опухоль, спайка, атрофия, дискинезия, гипертрофия и др.) желчных путей или желчного пузыря, приводящая к застою желчи (холестазу) как в печени, так и в желчном пузыре. Попадание в застоявшуюся желчь микроорганизмов или трематод создаёт наиболее благоприятные условия для холелитиаза, т.к. при этом к застоявшейся желчи добавляется слизь и погибшие эпителиальные клетки. Факторами риска камнеобразования также считаются ожирение, гемолитические анемии, нерациональное кормление, недостаточный моцион, наследственные факторы и др. [2, 4, 6, 9, 11, 13].
Камни во внутрипечёночных желчных путях у животных и человека встречаются гораздо реже, чем в желчном пузыре или во внепечёночных желчных протоках. Связано это с тем, что желчь в желчном пузыре является наиболее концентрированной и склонность к выпадению осадка проявляется в нём в первую очередь. Кроме того, желчь во внутри- и внепечёночных желчных путях постоянно движется (течет), а в желчном пузыре определённое время находится в покое.
Желчные камни по составу, внешнему виду резко отличаются между собой. В их химический состав в основном входят три вещества – холестерин, билирубинат кальция и карбонат кальция.
Различают три основных типа желчных камней:
— холестериновые камни. Состоят в основном из холестерина. Как правило, одиночные, желтовато-белого цвета, мягкой консистенции. Если камни долго находятся в пузыре, то они могут подвергнутся инкрустации солями кальция и стать комбинированными;
— пигментные камни. Состоят из билирубината кальция, холестерина и желчных кислот. Наиболее часто встречаются у собак. Они всегда множественные, чёрного цвета с блестящей поверхностью, фасетированного вида. Чаще рыхлой консистенции. Появление их связывают с избытком желчных пигментов, образующихся, в частности, при заболеваниях, сопровождающихся гемолизом;
— комбинированные (холестериново-пигментно-известковые) камни. В их состав входят все три компонента в различной пропорции и от преобладания какого-то из них зависят цвет и консистенция камней. Холестерин даёт желтоватый оттенок, билирубинат кальция – чёрно-бурый, карбонат кальция – белый. Комбинированные камни всегда множественные. Их поверхность обычно гладкая, форма неправильная, реже округлая. Если камней немного и они достаточно крупные, между ними образуются как бы суставные поверхности – слегка вогнутая на одном камне и соответственно выпуклая на соседнем.
При наличии любых камней имеется вероятность развития острого и хронического калькулёзного холецистита, хотя при холестериновых и пигментных камнях воспалительные процессы желчного пузыря встречаются редко.
Небольшие камни желчного пузыря при хроническом холецистите с расширением пузырного протока могут мигрировать из пузыря и в зависимости от их величины проскакивать в двенадцатиперстную кишку, застревать в пузырном протоке, общем желчном протоке или подниматься в печёночные протоки. Камень может действовать как клапан, затрудняющий приток желчи в двенадцатиперстную кишку или в желчный пузырь. В последнем случае вначале наступает спадение пузыря, затем абсорбция желчи и отёк стенки органа. Если же нарушается отток желчи от желчного пузыря, наступает переполнение пузыря желчью, нарушается кровообращение в нём в результате сдавливания питающих сосудов и развиваются деструктивные изменения в стенке органа. При наличии камней в протоках постоянно обнаруживают камни в пузыре или печени. Изолированного холедохолитиаза, по-видимому, не бывает. Если обнаружены камни в протоках и нет камней в пузыре или печени, можно предположить, что все камни вышли в протоки [1, 3, 12, 14, 15].
Обтекаемый камень желчных протоков может не вызывать клинических симптомов и морфологических изменений в протоках, желчном пузыре и в печени. Но чаще присутствие камня в протоке ведёт к серьёзным последствиям. В первую очередь возможно развитие механической (холестатической, обтурационной, подпечёночной) желтухи. При неполной обтурации может быть интермиттирующая желтуха, расширение лежащих выше отделов желчных путей и гипертрофия их стенок. Застой желчи распространяется и на внутрипечёночные желчные протоки, при длительной обтурации развивается вторичный билиарный цирроз печени, холангит. Полная обтурация желчных протоков обуславливает развитие симптомокомплекса острой механической желтухи, для которой характерны холемический синдром и синдром ахолии.
Холемический синдром развивается из-за попадания на фоне холестаза (приводящего к повышению давления в вышележащих желчных путях, растяжению и увеличению проницаемости желчных капилляров или их разрыву) в системный кровоток основных компонентов желчи. Клиническими проявлениями холемии являются желтуха (отложение билирубина придаёт слизистым оболочкам и склерам характерный иктеричный цвет), анорексия, рвота, дегидратация, болезненность при пальпации правого подреберья (вследствие спазма гладкой мускулатуры желчного пузыря и желчных протоков), брадикардия и кожный зуд (из-за повышения уровня желчных кислот в крови). При биохимическом анализе крови определяются высокие уровни общего билирубина, АЛТ, ЩФ и холестерина; при исследовании коагулограммы – снижение скорости свёртывания крови; при клиническом анализе крови возможен умеренный или выраженный лейкоцитоз (со сдвигом влево) или анемия.
Прекращение поступления желчи в кишечник (синдром ахолии) приводит к обесцвечиванию каловых масс, стеаторее, дисбактериозу и кишечной аутоинтоксикации [1, 3, 7, 8, 10, 11, 12].
Описание клинических случаев желчнокаменной болезни
У пациентов клиники «Биоконтроль» в течение первой половины 2009 г. было зарегистрировано три случая желчнокаменной болезни. У трёх животных (кошка породы корниш-рекс, пудель миниатюрный и йоркширский терьер) жалобы хозяев при первичном обращении были связаны с другими патологиями (пиометра, судорожный синдром, РМЖ и кашель), а при обследовании и дальнейшем лечении основного заболевания сопутствующим заболеванием был выявлен холелитиаз. Во всех трёх случаях диагноз был подтверждён патолого-анатомическим исследованием.
Клинический случай 1. Кошка, породы корниш-рекс, 11 лет, поступила на приём в клинику с жалобами владельцев на гнойные выделения из петли, периодическую рвоту желчью и анорексию в течение суток. Животному с установленным диагнозом – пиометра – была проведена надвлагалищная овариогистерэктомия. Через 12 дней после операции животное поступило на приём в крайне тяжёлом состоянии. Температура тела 32,0OС, бледные слизистые оболочки, вялость, анорексия, рвота желчью, судороги, жёсткие дыхательные шумы при аускультации.
Клинический анализ крови: лейкоциты – 32,8 тыс/мкл; эритроциты – 7,28 млн/мкл; гемоглобин – 101 г/л, гематокрит – 35,7%; тромбоциты – 58 тыс/мкл.
Биохимический анализ крови: глюкоза – 1,98 ммоль/л; билирубин — 9,9 мкмоль/л; АЛТ — 599 Ед/л; АСТ – 237 Ед/л; мочевина — 10,4 ммоль/л; креатинин — 190 мкмоль/л; панкреатическая амилаза – 1734 Ед/л.
При проведении УЗИ у животного обнаружили множество гиперэхогенных включений в печени и желчном пузыре. В тот же день кошке была выполнена диагностическая лапаротомия, при которой животному провели холецистотомию с удалением камней. Во время проведения операции у животного произошла остановка сердца.
При патолого-анатомическом исследовании обнаружены резкий отёк, острое воспаление печени (рис. 1); печёночный холелитиаз (рис. 2); межуточный нефрозо-нефрит; выраженный фиброз поджелудочной железы; отёк миокарда; ателектаз лёгких.

Рис. 1. Микрофото. Гистологический срез печени. Резкий отёк, лейкоцитарная инфильтрация. Окраска гематоксилином и эозином, об. ×40, ок. ×10

А

Б

В

Г
Рис. 2. Макрофото. Печёночный холелитиаз. Множество комбинированных камней жёлтого и тёмно-зелёного цвета во внутрипечёночных желчных путях. Камни легко «выдавливаются» при легком сдавливании печени, плотной консистенции (рис. А, Б, В). На распиле камня чётко видны слоистое строение и смена цвета (на рис. Г показана стрелкой)
Клинический случай 2. В клинику на приём поступила собака, породы пудель миниатюрный, самка, 17 лет с жалобами владельцев на судорожный синдром в течение суток. При клиническом осмотре – общее состояние животного тяжёлое. Температура тела 40OC. Слизистые оболочки цианотично-розовые. На ЭКГ – единичные экстрасистолы. Болезненность при пальпации брюшной стенки. При УЗИ были обнаружены пристеночные гиперэхогенные округлые образования диаметром до 0,3 см в полости желчного пузыря, диффузные изменения печени и признаки хронического нефрита.
Клинический анализ крови: лейкоциты – 23,5 тыс/мкл; эритроциты – 6,08 млн/мкл; гемоглобин – 128 г/л; гематокрит – 40,2%; тромбоциты – 752 тыс/мкл.
Биохимический анализ крови: глюкоза – 2,0 ммоль/л; билирубин – 0,9 мкмоль/л; АЛТ – 50 Ед/л; АСТ – 182 Ед/л; мочевина – 7,9 ммоль/л; креатинин – 78 мкмоль/л; панкреатическая амилаза – 559 Ед/л.
Животное было помещено в стационар клиники, где получало инфузионную терапию. У собаки наблюдались эпилептиформные приступы по 15-30 с каждые 2 ч. На 4-й день лечения в связи с крайне тяжёлым состоянием животного по желанию владельцев его подвергли эвтаназии.
При патолого-анатомическом исследовании обнаружено: массивное внутримозговое кровоизлияние в правую лобную долю головного мозга, умеренная внутренняя гидроцефалия (рис. 3); отёк, полнокровие, жировая дистрофия, периваскулярный склероз печени (рис. 4); холецистолитиаз (рис. 5); макронодулярный цирроз тела и головки поджелудочной железы; двусторонний крупноочаговый нефрозо-нефрит с циррозом и поликистозом; миокардит; сочетание эмфиземы, пневмосклероза и застойного полнокровия лёгких; гемосидероз селезёнки.

Рис. 3. Макрофото. Фронтальный срез головного мозга. Массивное внутримозговое кровоизлияние в правую теменную долю головного мозга (показано стрелкой), умеренная гидроцефалия
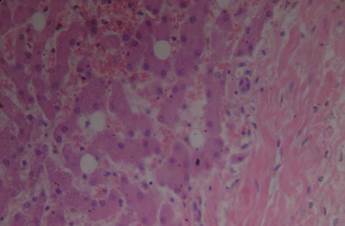
Рис. 4. Микрофото. Гистологический срез печени. Отёк, полнокровие, жировая дистрофия, периваскулярный склероз печени. Окраска гематоксилином и эозином, об. ×40, ок. ×10


Рис. 5. Макрофото. Холецистолитиаз. Множественные пигментные камни диаметром до 4 мм (на рис. А показаны стрелкой) в неизменённом желчном пузыре, рыхлой консистенции, крошащиеся при умеренном сдавливании (рис. Б).
Клинический случай 3. На приём в клинику поступила собака, породы йоркширский терьер, самка, возраст 5 лет с жалобами владельцев на новообразование молочной железы (замеченное 6 мес. назад) и кашель в течение 3-х месяцев, усиливающийся после физической нагрузки. При клиническом исследовании установлено: РМЖ II стадия, слизистые оболочки цианотичные, трахеальный рефлекс резко положительный, дыхание чистое, везикулярное. При УЗИ – гиперэхогенное содержимое в просвете желчного пузыря (рис. 6), двусторонний нефролитиаз, диффузные изменения печени. При рентгенологическом исследовании: увеличение правых отделов сердца, коллапс трахеи.
А 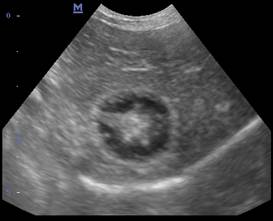
Б 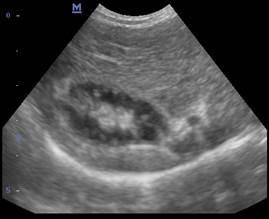
Рис. 6. Ультрасканограмма желчного пузыря в поперечном (а) и продольном (б) сечениях. Гиперэхогенное содержимое в просвете желчного пузыря (показано стрелкой)
Животное проходило лечение в клинике в течение 4-х месяцев: прохождение курса лучевой терапии, с дальнейшим проведением регионарной мастэктомии и трёх курсов химиотерапии. Ухудшение состояния наступило после окончания курса химиотерапии: стойкая панцитопения, эпилептиформные приступы, желудочно-кишечное кровотечение.
В связи с крайне тяжёлым состоянием животного по желанию владельцев его подвергли эвтаназии.
Патолого-анатомический диагноз: выраженная внутренняя гидроцефалия (рис. 7), жировая дистрофия печени (рис. 8, 9), холецистолитиаз (рис. 10), тромбоз полости правого желудочка, коллапс трахеи III степени, двусторонний нефролитиаз, точечные кровоизлияния в тонком и толстом отделах кишечника.

Рис. 7. Макрофото. Сегментальный срез головного мозга. Расширение желудочков головного мозга

Рис. 8. Макрофото. Жировая дистрофия печени. Желтоватого цвета орган на разрезе
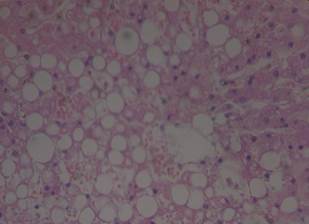
Рис. 9. Микрофото. Жировая дистрофия печени. Многочисленные жировые капли в цитоплазме гепатоцитов, создающие мелкосетчатый рисунок. Окраска гематоксилином и эозином, об. ×40, ок. ×10
А 
Б 
Рис. 10. Холецистолитиаз. Пигментные камни желчного пузыря на рис. А показаны стрелками. Камни рыхлой консистенции, крошатся от умеренного
