Жидкость после удаления рака желудка
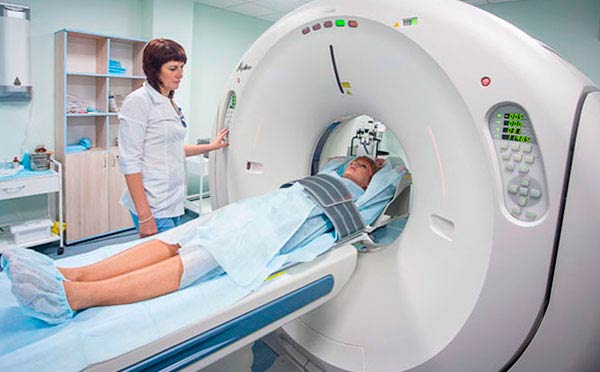
Асцит – самое частое осложнение рака желудка. Скопление жидкости в брюшной полости может оказаться первым признаком онкологического заболевания, позволяющим обратить внимание на неблагополучие в организме. Но чаще всего асцит развивается в метастатической стадии рака.
Большая часть пациентов с метастазами имеют асцит той или иной степени выраженности.
Почему появляется асцит?
Распространение отсевов опухоли по брюшине может привести к выработке большого количества жидкости. Нет закономерности между размерами или количеством опухолевых узлов и скоростью накопления, а также количеством вырабатываемой жидкости. Источник образования экссудата – кровеносная капиллярная сеть листков брюшины, всасывание осуществляют лимфатические сосуды.
Существуют два основных механизма асцита:
- Метастазы по брюшине увеличивают проницаемость кровеносных и вызывают обструкцию лимфатических сосудов, которые в норме способны вывести жидкости в 20 раз больше, чем выработалось.
- Нарушение оттока лимфы при опухолевом поражении лимфатических узлов брюшной полости, когда изменённые лимфоузлы не могут «качать» лимфу по сосудам.
Как проявляется асцит при раке желудка?
Минимальный по объёму асцит выявляют только при инструментальном исследовании – УЗИ или КТ брюшной полости. Умеренный асцит, начиная с объёма жидкости более литра-полутора, врач определит при обычном осмотре. УЗИ брюшной полости позволит определить объём экссудата.
Пациент замечает неблагополучие только при значительных количествах, потому что симптомы нарастают постепенно. Довольно долго организм способен адаптироваться к нарастающему в брюшной полости объёму жидкости. Остаётся без должного внимания и увеличение окружности талии – его относят на счёт метеоризма или прибавки веса.
При избытке жидкости в брюшной полости поднимается купол диафрагмы, что затрудняет глубокое дыхание, нарушается вентиляция нижних отделов лёгких и возможна активизация инфекции дыхательных путей.
Повышение внутрибрюшинного давления усугубляет лёгочно-сердечную недостаточность, приводит к тошноте и рвоте при приёме небольшого количества пищи и воды. Прогрессирует варикозное расширение геморроидальных вен и отёчность нижних конечностей.
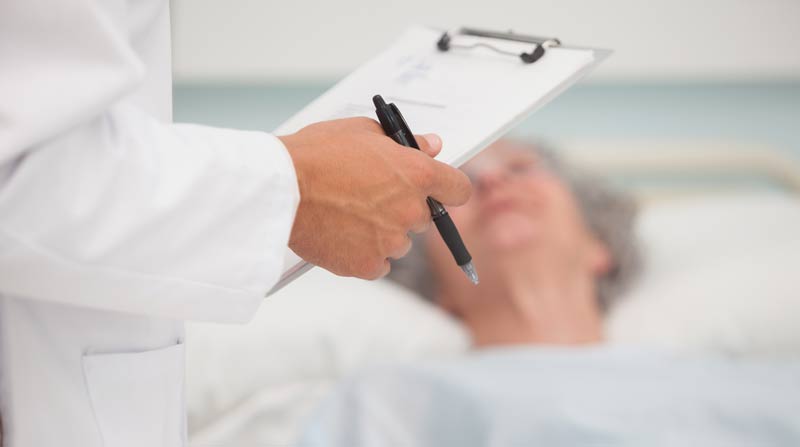
Как бороться с асцитом?
На первом этапе асцит пытаются уменьшить сокращением выпиваемой жидкости и употребления пищевой соли, приёмом мочегонных препаратов. Результаты такой терапии более чем скромные, поскольку опухолевые узлы продолжают выработку патологической жидкости. Вторым номером во всех национальных рекомендациях по лечению асцита идёт удаление жидкости через небольшой прокол передней брюшной стенки – лапароцентез.
До настоящего времени не удалось предложить более действенного способа борьбы с асцитом, чем лапароцентез, хоть обеспечение самой манипуляции существенно улучшилось. Технически без особой сложности можно удалить всю накопившуюся жидкость, сколько бы её ни было. За один приём организм способен перенести выведение около 5-6 литров жидкости.
Утрата большего объёма изменит давление в брюшной и грудной полостях, что бесследно не пройдёт, ведь за несколько минут органы радикально поменяют своё положение, приток крови в сосуды увеличится. Пациент испытает ощущения падения в «воздушную яму», из которой не выбраться без реанимационных мероприятий.
Классическая медицина предлагает удаление большого асцита за несколько этапов, к примеру, за несколько дней, каждый раз заново выполняя новый прокол брюшной стенки. Сегодня имеется возможность щадящего постепенного выведения большого количества жидкости – с помощью установки специальной перитонеальной порт-системы, что физиологично – жидкость выводится медленными темпами, как и накапливалась, а смещённые органы постепенно встают на определённое природой место.
Проблема дефицита белков
В асцитической жидкости содержится большое количества белка – более 30 грамм в литре, который худо-бедно всасывается из брюшной полости, хоть и не способен ликвидировать дефицит, но всё-таки какие-то граммы участвуют в жизнедеятельности организма. При лапароцентезе белок теряется безвозвратно – с каждым литром 30 грамм. Получается замкнутый круг, когда из-за значительного ухудшения состояния невозможно не удалять жидкость, но и удаление даёт малое облегчение, так как вместо признаков сдавления и смещения органов приходят симптомы усугубления белковой недостаточности.
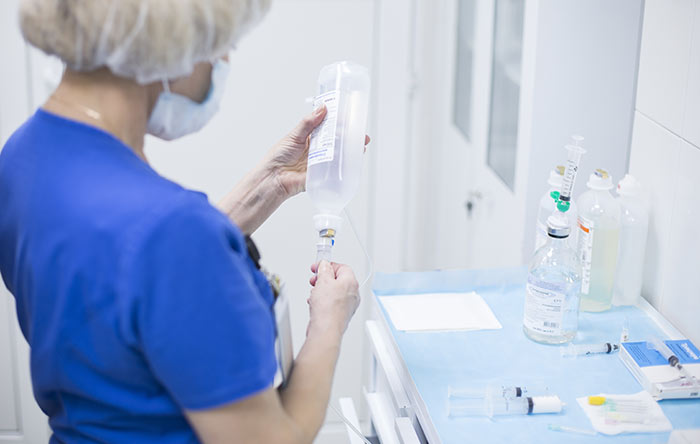
Часть потерянного с асцитической жидкостью белка способен восполнить альбумин, вводимый внутривенно. Стоимость альбумина довольно высокая, но это неустранимая неизбежность. Более дешёвые небелковые препараты позволяют компенсировать утраченный сосудистым руслом объём жидкости, но не влияют на дефицит белков крови. Контролируют достаточность внутривенной инфузии альбумина по анализам крови на содержание белков.
Возможно ли радикальное лечение асцита?
Хирургическое удаление метастатических узлов, разбросанных опухолью по всем листкам брюшины нереально. Во время оперативного вмешательства по поводу первичного рака желудка практикуют удаление листков брюшины с очень мелкими метастазами и на ограниченном пространстве. Для такой манипуляции необходимо условие: метастаз должен ограничиваться только самим серозным листком, ни клетки опухоли не должно прорасти в окружающие ткани, а опухоль имеет низкую степень злокачественности.
Химиотерапия при асците
Успехи химиотерапии при раке желудка скромны, но они есть. Ещё десять лет назад введение цитостатиков в брюшную полость после удаления излишней жидкости признавалось нецелесообразным. И дело не в отсутствии разительных позитивных результатов – токсические реакции на лекарственные средства ухудшали и без того плохое самочувствие пациента.
Основная причина неудовлетворённости внутрибрюшинной химиотерапией была не столько в недостатках самих лекарств, сколько в невозможности создания условий для их оптимального контакта с опухолью: концентрация препарата снижалась постоянно пребывающим экссудатом, а частота введения цитостатика была ограничена необходимостью каждый раз заново выполнять лапароцентез.
Сегодня интраперитонеальная – внутрибрюшинная химиотерапия с помощью лапаропортов считается одним из перспективных направлений современной терапии.
Во время небольшой операции имплантационная порт-система устанавливается в передней брюшной стенке на уровне VIII-IX межреберья и фиксируется к рёберной дуге, что в дальнейшем позволяет создавать более высокую концентрацию химиотерапевтических препаратов в брюшной полости.
В клинических исследованиях в брюшной полости удавалось создавать в 20 раз более высокую концентрацию препаратов платины и в 1000 раз таксанов с более длительной экспозицией. Естественно, часть препарата всасывается, что сопряжено с токсическими реакциями, но качественная симптоматическая терапия и квалифицированное сопровождение лечения – «дело техники» наших врачей.
Цены в Европейской онкологической клинике на эвакуацию асцита (лапароцентез)
В Европейской онкологической клинике действует специальное предложение на дренирование асцита в условиях дневного стационара – 50000 руб.
В цену включено:
- Осмотр и консультация хирурга-онколога.
- Общий анализ крови, биохимический анализ крови, ЭКГ.
- УЗИ органов брюшной полости с определением уровня свободной жидкости
- Проведение лапароцентеза с УЗИ навигацией.
- Комплексная медикаментозная терапия, направленная на восстановление водно-электролитного баланса.
Удаление жидкости из брюшной полости проводится с применением наиболее современных методик, передового опыта российских и зарубежных врачей. Мы специализируемся на лечении рака и знаем, что можно сделать.
Источник
Асцит — патологическое состояние, при котором в брюшной полости скапливается жидкость. Причины его бывают различными. Чаще всего к асциту приводит цирроз печени. Так же он возникает как осложнение онкологических заболеваний, при этом ухудшается состояние больного, снижается эффективность лечения.
Некоторые цифры и факты:
- На ранних стадиях онкологических заболеваний умеренный асцит развивается примерно у 15–50% пациентов;
- Тяжелый асцит развивается примерно у 7–15% онкологических больных;
- При асците в брюшной полости может скапливаться до 5–10 литров жидкости, в тяжелых случаях — до 20 литров.
При каких видах рака может развиваться асцит?
Чаще всего асцит развивается при следующих онкологических заболеваниях:
- рак яичников;
- рак печени;
- рак поджелудочной железы;
- рак желудка и кишечника;
- рак матки;
- рак молочной железы;
- неходжкинские лимфомы, лимфома Беркитта.
Почему рак приводит к скоплению жидкости в брюшной полости?
При раке печени причины асцита те же, что при циррозе (собственно, рак печени в большинстве случаев и развивается на фоне цирроза): нарушение оттока крови, повышение давления и застой в венах, нарушение синтеза альбумина и снижение онкотического давления крови.
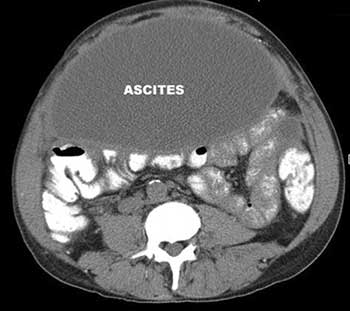
При злокачественных опухолях других органов (желудка, кишечника, матки, яичников) асцит возникает из-за поражения раковыми клетками брюшины. Из-за этого нарушается всасывание жидкости. Если опухолевые клетки поражают лимфатические узлы, асцит может возникать из-за нарушения оттока лимфы.
Проявления асцита при онкологических заболеваниях
Если в брюшной полости скапливается небольшое количество жидкости (100–400 мл), симптомы отсутствуют. В таких случаях асцит обнаруживают зачастую случайно во время УЗИ или КТ органов брюшной полости.
Постепенно, по мере нарастания асцита, живот увеличивается в объеме. Пациент чувствует тяжесть в животе, ноющие боли. За счет задержки жидкости увеличивается масса тела. Происходит сдавление внутренних органов, возникают такие симптомы асцита брюшной полости, как тошнота и рвота, отрыжка, расстройство стула и мочеиспускания. Изменяется внешний вид пупка: он выбухает, как во время беременности. Больной чувствует слабость, постоянную усталость, снижается аппетит.
К каким осложнениям приводит асцит?
При выраженном, длительно существующем асците жидкость скапливается в плевральной полости, развивается гидроторакс. Это приводит к еще большему расстройству дыхания, тяжелой одышке.
*По аналогии с брюшной полостью, в грудной клетке находится тонкая оболочка из соединительной ткани — плевра, париетальный листок которой выстилает стенки, висцеральный покрывает легкие.
При портальной гипертензии микроорганизмы из кишечника могут проникать в асцитическую жидкость. Развивается спонтанный бактериальный перитонит. Ситуация усугубляется тем, что в асцитической жидкости мало антител, поэтому иммунный ответ слабый.
Редкое, но очень тяжелое осложнение асцита — гепаторенальный синдром. При этом цирроз и печеночная недостаточность приводят к серьезному нарушению функции почек, вплоть до тяжелой почечной недостаточности. Пациенты с гепаторенальным синдромом в среднем живут от 2 недель до 3 месяцев. Причины этого состояния до конца не известны. Считается, что кровоток в почках нарушается из-за чрезмерного применения мочегонных средств, внутривенных контрастов во время рентгенографии и компьютерной томографии, некоторых лекарственных препаратов.
Методы диагностики
Внешние признаки асцита становятся хорошо заметны, когда количество жидкости в брюшной полости достигает 0,5–1 литра. Живот при этом заметно увеличен. Когда пациент стоит, он выглядит отвисшим, в положении лежа — распластан, боковые его части выступают. Врачи называют такую картину образно «животом лягушки».
Если во время осмотра врач обнаруживает у пациента признаки асцита, он может назначить следующие методы диагностики:
- УЗИ, КТ и МРТ помогают диагностировать асцит и оценить количество жидкости в брюшной полости, состояние внутренних органов, обнаружить злокачественную опухоль, оценить количество, размеры, локализацию патологических очагов, степень прорастания опухоли в различные органы и ткани;
- Биохимический анализ крови помогает оценить функцию печени, почек, определить уровни электролитов, степень снижения количества белка;
- Исследование свертываемости крови помогает выявить нарушения, связанные с расстройством функции печени (печень синтезирует некоторые факторы свертывания);
- Диагностический лапароцентез — процедура, во время которой проводят пункцию брюшной полости под контролем УЗИ и получают небольшое (примерно столовую ложку) количество асцитической жидкости. В ней исследуют уровни лейкоцитов и эритроцитов, общего белка и альбумина, глюкозы, амилазы. Проводят анализы на присутствие микроорганизмов, цитологическое исследование на предмет наличия опухолевых клеток.

Лечение асцита в онкологии
Лечение асцита у онкологических больных — сложная задача. От правильного подхода к ее решению зависит качество и продолжительность жизни пациента, эффективность противоопухолевой терапии. В идеале нужна клиника, которая специализируется на лечении асцита у онкобольных.
Консервативное лечение
Такая терапия помогает выводить до 1 литра жидкости в сутки. Она существенно улучшает состояние примерно у 65% пациентов. Но применять ее можно только при умеренном асците. Многие пациенты на поздних стадиях рака плохо переносят ограничение жидкости и соли. Поэтому консервативная терапия не рассматривается как основной метод лечения асцита при онкологии.
Лапароцентез
Лапароцентез — процедура, во время которой в брюшную полость под контролем УЗИ вводят троакар — специальный инструмент в виде трубки с острыми краями (напоминает иглу, только толще) и выводят жидкость. Лапароцентез проводят под местной анестезией в стерильных условиях, во время процедуры пациент сидит или лежит. Троакар вводят по средней лини живота или по линии, которая соединяет пупок с подвздошной костью. Во время процедуры из брюшной полости можно безопасно вывести до 5–6 литров жидкости.
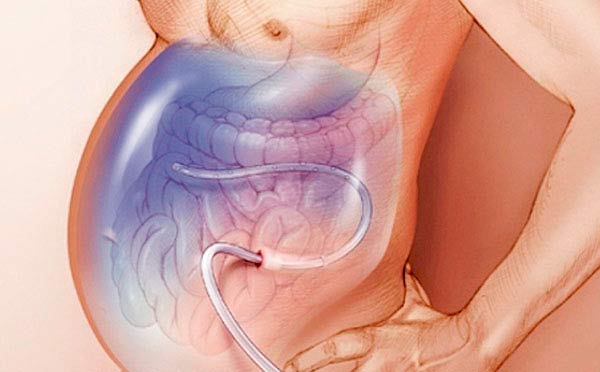
После лапароцентеза врач может установить в брюшную полость перитонеальный катетер — трубку, соединенную с резервуаром для оттока асцитической жидкости. При выраженном асците катетер может быть оставлен на несколько дней.
Возможные осложнения во время и после лапароцентеза:
- Падение артериального давления при выведении большого количества жидкости. Для того чтобы этого не произошло, асцитическую жидкость выводят медленно, постоянно контролируют пульс и артериальное давление пациента;
- Белковая недостаточность из-за потери большого количества альбуминов вместе с асцитической жидкостью. Для борьбы с белковым дефицитом внутривенно вводят альбумин;
- Боль. При необходимости после лапароцентеза назначают обезболивающие препараты.
- Жидкость, которая остается после процедуры в некоторых отделах брюшной полости. Для того чтобы вывести всю жидкость, врач может установить более одного перитонеального катетера в разных местах.
- Перитонит в результате проникновения микроорганизмов в брюшную полость. Редкое осложнение. Для его профилактики и лечения назначают антибактериальные препараты, может потребоваться хирургическое вмешательство.
- Нарушение оттока жидкости по перитонеальному катетеру. Чаще всего возникает из-за того, что конец катетера «присосался» к стенке брюшной полости или внутренним органам. Зачастую, чтобы справиться с этой проблемой, достаточно изменить положение тела. Если это не помогает, может потребоваться замена катетера.
- Выделение жидкости после удаления катетера. Для ее сбора на 1–2 дня на место пункции накладывают специальный резервуар.
- Сращение сальника (части брюшины) или участка кишки с брюшной стенкой возникает при повторных пункциях. Если это приводит к значительному нарушению работы кишки, может потребоваться хирургическое рассечение спаек.
Внутрибрюшинная химиотерапия
Некоторым пациентам назначают внутрибрюшинную химиотерапию — химиопрепарат вводят в высоких дозах в брюшную полость, иногда предварительно нагрев его до 41 градуса (такую химиотерапию называют гипертермической). Это помогает уменьшить асцит. Проводят системную химиотерапию.
Один из новых препаратов для лечения асцита у онкологических больных — моноклональное антитело Катумаксомаб. Его также вводят внутрибрюшинно. Катумаксомаб взаимодействует с рецепторами опухолевых и иммунных клеток и индуцирует иммунную реакцию. Но препарат действует лишь на раковые клетки, обладающие определенными молекулярно-генетическими характеристиками.
Хирургическое лечение
Некоторым пациентам показана оментогепатофренопексия. Во время этой операции сальник подшивают к печени или диафрагме. Благодаря возникновению такого контакта улучшается всасывание асцитической жидкости.
В качестве паллиативного хирургического вмешательства прибегают к перитонеовенозному шунтированию. В брюшную полость устанавливают катетер, который соединяет ее с венозной системой. Катетер оснащен клапаном — он открывается, когда давление в брюшной полости превышает центральное венозное давление. При этом происходит сброс жидкости в вены.
Деперитонизация стенок брюшной полости — вмешательство, во время которого хирург удаляет участки брюшины, тем самым создавая дополнительные пути для оттока асцитической жидкости.
Применяются и другие виды хирургического лечения.
Прогноз при асците у онкологических больных
Обычно асцит возникает на поздних стадиях рака, ухудшает прогноз для онкологического пациента. При злокачественных опухолях, осложнившихся асцитом, отмечается низкая выживаемость. Паллиативное лечение помогает улучшить качество жизни, несколько увеличить ее продолжительность. Врач должен тщательно оценить состояние пациента, выбрать оптимальные методы лечения, исходя из их потенциальной эффективности и рисков.
Цены
В Европейской клинике действует специальное предложение на дренирование асцита в условиях дневного стационара – 50000 руб.
В цену включено:
- Осмотр и консультация хирурга-онколога.
- Общий анализ крови, биохимический анализ крови, ЭКГ.
- УЗИ органов брюшной полости с определением уровня свободной жидкости
- Проведение лапароцентеза с УЗИ навигацией.
- Комплексная медикаментозная терапия, направленная на восстановление водно-электролитного баланса.
Удаление жидкости из брюшной полости проводится с применением наиболее современных методик, передового опыта российских и зарубежных врачей. Мы специализируемся на лечении рака и знаем, что можно сделать.
Источник
Удаление желудка или гастрэктомия — травматичное вмешательство, трудно дающееся больному и оставляющее пожизненные осложнения, но рак желудка не имеет шансов на излечение, если операцию не делать.
До операции онкологический больной редко думает, как жить после удаления желудка, ему важно быстро избавиться от опухоли, чтобы выжить. После хирургического лечения приходит понимание, что отсутствующий орган не заменят искусственным, и проблем со здоровьем уже не избежать.
Показания для операции удаления желудка при раке
Современная онкология стремится свести к минимуму объем удаляемых тканей, чтобы минимизировать осложнения после операции и последующие страдания пациента, тем не менее полное удаление желудка одна из самых частых операций при раке.
Гастрэктомия выполняется при опухоли, как 1, так и 3 стадии, абсолютное противопоказание для хирургического вмешательства — наличие отдалённых метастазов рака.
Гастрэктомию проводят, когда операция меньшего объёма невыполнима или не гарантирует отсутствие рецидива. Гастрэктомия — это последняя возможность для спасения, иным способом карциному излечить не удается.
Только в одном случае при 4 стадии желудочной карциномы существует относительное противопоказание к хирургии — метастазирование в яичник. Относительное оттого, что при возможности удаления первичной опухоли и пораженного метастазами яичника, одномоментно выполняется сразу две операции: гастрэктомия и овариэктомия, иногда и вместе с маткой. Но если что-то удалить невозможно, хирургический этап лечения заменяется на химиотерапию.
Как удаляют желудок при раке?
Подход к желудку через брюшную стенку — оперативный доступ – зависит от состояния пациента и протяженности опухолевого процесса в пищеводе. Во время операции пищевод пересекается на 5–7 сантиметров выше опухоли, полностью удаляется желудок и сальниковые сумки с лимфатическими узлами. В брюшной полости не должно остаться ни единого опухолевого очага.
Типичные разрезы кожи и мягких тканей живота:
- Классический разрез проходит по средней линии живота — это срединная лапаротомия.
- В некоторых случаях прибегают к продлению разреза с живота на грудную стенку — это тораколапоротомия.
- При необходимости удаления значительного участка пораженного пищевода дополнительно к срединной лапаротомии делают разрез между ребрами.
- К пораженному раком пищеводу можно подобраться и изнутри — через диафрагму, что возможно и при классическом доступе.
Какой оперативный доступ при удалении лучше
Не существует стандартов, определяющих где и сколько надо разрезать брюшной стенки и как далеко продвинуться в грудной полости, всё базируется на индивидуальных особенностях конкретного пациента и опухолевого поражения.
Хирург-онколог самостоятельно выбирает хирургический доступ, при максимальном обзоре поля деятельности позволяющий минимальное повреждение здоровых тканей и оптимальную технику операции, снижающую возможность осложнений после удаления желудка.
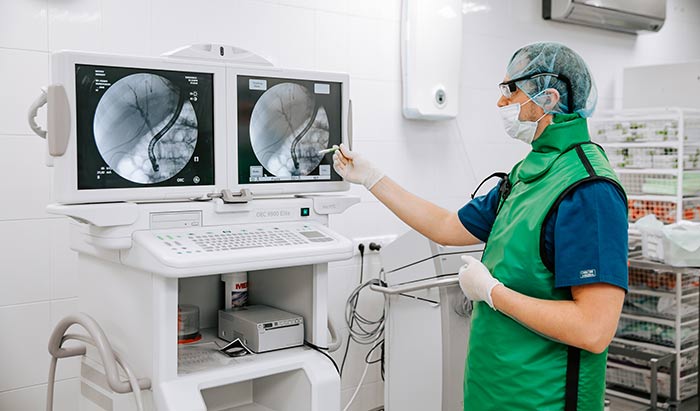
Сегодня при раннем раке открытые операции успешно заменяются эндоскопическими технологиями, лапароскопическая гастрэктомия, несомненно, технически сложнее, но для пациента выгоднее, поскольку не увеличивает осложнения после операции, восстановление пациента проходит быстрее.
Способ доступа к больному органу и методику операции определяет хирург-онколог, его выбор отражает практический хирургический опыт и персональные навыки, не сомневайтесь, профессиональная квалификация специалистов нашей клиники всегда на уровне «высший класс».
Этапы удаления желудка
Ход операции удаления всего или только части органа (резекции) протекает по одному плану, но с разным объёмом удаляемых тканей.
- Сначала проводится мобилизация — отсечение органа от фиксирующих его внутренних связок, перевязка питающих артерий и вен. Одновременно проводится тщательный осмотр органов брюшной полости и на основе увиденного в план операции вносятся коррективы.
- Второй этап — собственно удаление, с отсечением желудка от пищевода и двенадцатиперстной кишки. При вовлечении в опухолевый конгломерат близлежащих органов брюшной полости, в том числе диафрагмы или печени, поджелудочной железы или толстого кишечника, если технически возможно, выполняются сложные и объемные комбинированные операции, то есть гастрэктомия и, например, резекция поджелудочной железы или печени.
- Третий этап — восстановление пищеварительного тракта, то есть соединение пищевода с кишечником, что обеспечит в дальнейшем передвижение пищи.
Восстановление после операции
Рак желудка приводит к серьёзным внутриклеточным изменениям, нарушаются все биохимические процессы, поскольку организм не получает необходимых ему веществ из-за нарушения всасывания в желудочно-кишечном тракте. Ещё несколько десятилетий назад после гастрэктомии погибал каждый четвёртый пациент, сегодня осложнения и смертность сведены к минимальным показателям.
Послеоперационное восстановление очень индивидуально, на нем сказывается возраст и пол пациента, существующие у него хронические болезни и степень нарушений, обусловленных карциномой, вовлечение других органов брюшной полости и «живой» вес больного. На длительности восстановления отражается даже время года, так лето не самое благоприятное время для хирургических манипуляций.
Главное для больного — не торопиться после удаления желудка побыстрее покинуть клинику, так как незавершенность лечебных мероприятий впоследствии откликнется проблемами со здоровьем, которые могут основательно испортить жизнь.
Осложнения после операции при раке
Ранние осложнения немногочисленны, но при несвоевременном выявлении могут быть фатальными для пациента.
Несостоятельность швов в месте соединения пищевода с кишкой — в анастомозе — возникает не оттого, что хирург «что-то не то сделал», а обусловлена недостаточностью внутренних резервов организма, нарушениями гомеостаза, слабостью иммунной защиты и неполноценностью питания — нутритивным статусом до лечения. Частота этого осложнения колеблется от 2% до 10%.
Нарушение оттока панкреатических секретов из-за отечности поджелудочной железы может привести к развитию острого панкреатита. На частоте панкреатита сказывается хирургическая техника, но определяющую роль играет объем удаленных тканей и исходное состояние органов желудочно-кишечного тракта. Главное — вовремя диагностировать осложнение и проводить адекватную медикаментозную профилактику.

Несостоятельность швов и панкреатит способны инициировать воспалительные процессы внутри брюшной полости, в частности, абсцесс или перитонит, кишечную непроходимость или локальное скопление жидкости.
Процент перечисленных патологических послеоперационных состояний небольшой, а в нашей клинике значительно ниже средних статистических величин, потому что на результате отражается талант и опыт хирурга-онколога в сочетании с отличными диагностическими возможностями.
Реабилитация после удаления желудка при раке
Переоценить значение восстановительных мероприятий после гастрэктомии невозможно, по большому счёту хорошее самочувствие «приходит» к пациенту через месяц после выписки из больницы. Если попытаться коротко ответить на вопрос «как живут после удаления желудка», то однозначно неважно, когда живут без помощи специалистов.
Рана зарастёт, но восстановление нормального питательного нутритивного статуса в измененном пищеварительном тракте проходит сложно — просто протертая и на пару приготовленная еда проблему не решает. А проблема сцеплена с недостаточностью иммунитета и отсутствием полноценного всасывания необходимых для организма питательных элементов.
Для скорейшего восстановления и продолжения противоопухолевого лечения требуется индивидуальная программа реабилитационных мероприятий.
Прогноз после удаления желудка
Онкологическая статистика знает, сколько живут больные карциномой желудка в зависимости от стадии. Нет литературных данных, сокращает ли жизнь удаление важнейшей части пищеварительного тракта, но точно известно, что продолжительность жизни больного зависит от распространенности первичной карциномы и биологических характеристик раковых клеток — дифференцировки, их чувствительности к химиотерапии и сопутствующих заболеваний.
Онкологическая наука очень точна, она знает, какой алгоритм диагностических исследований необходим при заболевании, сколько процентов больных разными стадиями и сколько лет в среднем живут, может предложить целый комплекс лечебных мероприятий при определенных морфологических характеристиках карциномы.
Одного не может онкология — дать конкретному пациенту рецепт оптимального лечения с точным расписанием необходимых ему манипуляций и процедур. Но это могут сделать и делают опытные онкологи Европейской клиники.
Список литературы
- Давыдов М.И., Туркин И.Н., Полоцкий Б.Е./Современная хирургия рака желудка: от D2 к D3// Материалы IX Российского онкологического конгресса; Москва 2005.
- Стилиди И.С., Неред С.Н./Современные представления об основных принципах хирургического лечения местно-распространенного рака желудка // Практическая онкология; 2009; Т.10, № 1.
- Янкин A.B./Современная хирургия рака желудка //Практическая онкология;2009; Т. 10, № 1.
- Curcio G., Mocciaro F., Tarantino I. et al./Self-Expandable Metal Stent for Closure of a Large Leak after Total Gastrectomy //Case Rep. Gastroenterol.;2010; № 4.
- Etoh T., Inomata M., Shiraishi N., Kitano S./Revisional Surgery After Gastrectomy for Gastric Cancer //Surg. Laparosc. Endose. Percutan. Tech.;2010.;v. 20, № 5.
- Isgiider A.S., Nazli O., Tansug T., et al/ Total gastrectomy for gastric carcinoma// Hepatogastroenter.; 2005; v. 52.
- Zhang C.H., Zhan W.H., He Y.L. et al. /Spleen preservation in radical surgery for gastric cardia cancer //Ann. Surg. Oncol.; 2007; v. 14.
Источник
