Канцеропревенция при раке желудка

Елена Александровна Полуэктова, врач, кандидат медицинских наук:
– Слово предоставляется Татьяне Львовне Лапиной, «Актуальные вопросы канцерпревенции».
Татьяна Львовна Лапина, доцент, кандидат медицинских наук:
– Спасибо большое, Елена Александровна. Итак, актуальные вопросы канцерпревенции – речь идет, конечно, о профилактике рака желудка.
Безусловно, нужно говорить о том, что мы понимаем, что канцерпревенция возможна, потому что есть устранимые факторы риска рака желудка. И на первое место среди устранимых факторов риска рака желудка, конечно, нужно вынести инфекцию пилорического хеликобактера. И мы видим, что действительно это тот фактор риска, который реально связан с инфекцией пилорического хеликобактера.
Итак, наличие хронического гастрита, вызванного инфекцией пилорического хеликобактера, повышает риск рака желудка в 6 раз. Это гораздо более актуально, чем вклад, например, изменения рациона питания в риск рака желудка. И поэтому абсолютно ясно, что вопросы канцерпревенции, профилактики рака желудка, сейчас неотъемлемы от вопросов ведения пациентов с инфекцией пилорического хеликобактера.
И поэтому последний европейский консенсус, созданный благодаря специалистам европейской группы по изучению хеликобактера (это IV Маастрихтский консенсус), в качестве одного, наверное, из своих ключевых разделов называет раздел, который озаглавлен как «Предотвращение рака желудка». И европейская группа по изучению пилорического хеликобактера провозглашает инфекцию пилорического хеликобактера как наиболее доказанный фактор риска рака желудка.
И, соответственно, эксперты (посмотрите, пожалуйста) с высоким уровнем научной доказательности «1a», с высокой степенью рекомендации «A» говорят о том, что элиминация пилорического хеликобактера служит самой многообещающей стратегией для снижения заболеваемости раком желудка.
Идеологическая основа такого положения, идеологическая основа этой стратегии лежит, конечно, на признании так называемого «каскада Корреа». Пелайо Корреа сформулировал вот такую изящную схему последовательных этапов патогенеза рака желудка. И понятно, что от хронического гастрита через трофический гастрит и кишечную метаплазию проходят пути длительного процесса, которые могут закончиться формированием дисплазии и рака желудка.
Вы видите типичные морфологические примеры: хронический активный хеликобактерный гастрит, атрофический гастрит (вы видите здесь совершенно четкие признаки наличия кишечной метаплазии у пациента), и последний фрагмент – это диспластически измененный эпителий, причем это, конечно, выраженная степень дисплазии слизистой оболочки.
Одно из очередных положений IV Маастрихтского консенсуса гласит: гистопатологические изменения на морфологическом уровне указывают на то, что рак желудка редко развивается без хронического активного гастрита, и объем поражения, и степень гастрита с атрофией и кишечной метаплазией ассоциированы с раком желудка. Собственно, здесь, конечно, действительно, вот эти положения в русле концепции «каскада Пелайо Корреа», естественно, были высказаны.
Что нам дает эрадикация инфекции пилорического хеликобактера? Почему мы говорим о возможности канцерпревенции с помощью элиминации инфекции пилорического хеликобактера? Все дело в том, что эрадикация пилорического хеликобактера ликвидирует воспалительный ответ, замедляет, а, возможно, и останавливает прогрессию атрофии. Более того, некоторые авторы даже говорят о возможности обратного развития атрофических изменений после эрадикации инфекции пилорического хеликобактера. Соответственно, имеются веские доказательства в пользу того, что эрадикация пилорического хеликобактера снижает риск рака желудка.
И этому есть определенные научные доказательства, даже не в виде разрозненных исследований, а мы перешли уже на очередной уровень научной доказательности, более высокий, более достоверный. Речь идет о наличии метаанализов клинических исследований. И при создании Маастрихтского консенсуса эксперты, в том числе, использовали данные вот этого метаанализа.
И вы видите, что здесь перечислены работы, выполненные в Японии и в основном, конечно, в других азиатских странах. Я должна сказать, что, наверное, страны Азиатского региона действительно во многом задают тон в представлении об эрадикации пилорического хеликобактера как радикальной мере профилактики рака желудка. В результате проведения этого метаанализа делается вывод, что эрадикация пилорического хеликобактера может снизить заболеваемость раком желудка в популяции на одну треть.
Можно ли говорить о том, что эрадикация пилорического хеликобактера вообще снизит риск рака желудка у конкретного пациента до нуля? Конечно, нет. И в первую очередь нужно иметь в виду, на каком этапе проведена эрадикационная терапия инфекции пилорического хеликобактера. Потому что если эрадикационная терапия инфекции пилорического хеликобактера была проведена уже на этапе формирования атрофического гастрита, даже после успешной эрадикации пациент с атрофическим гастритом останется в группе риска по раку желудка, и его нужно будет соответствующим образом наблюдать.
Каким образом наблюдать, с каким интервалом, какие методы применять? В первую очередь нужно говорить о том, что мы можем стратифицировать большие группы людей, в зависимости от выраженности факторов риска рака желудка, по простым серологическим маркерам. И в первую очередь здесь речь идет, конечно, о маркере атрофии тела желудка – о сывороточном пепсиногене. Низкий сывороточный пепсиноген – значит, выраженный атрофический гастрит, значит, более высок риск рака желудка.
И таким образом, например, в Японии предлагается переключиться с модели скрининга, которая в Японии уже существует. Вы знаете, что эта модель скрининга двухступенчатая, то есть группа риска для проведения последующей гастроскопии вычленяется из популяции благодаря рентгенологическому исследованию желудка, барий с двойным контрастированием.
И в настоящее время идет подготовительная работа к тому, чтобы по-другому проводить скрининг рака желудка и, в зависимости от наличия инфекции пилорического хеликобактера и антител к инфекции пилорического хеликобактера, в зависимости от наличия маркера атрофии тела желудка, планировать длительность и периодичность эндоскопического наблюдения за этими больными. И вы видите, что в любом случае пациентам с инфекцией пилорического хеликобактера назначается эрадикационная терапия.
Если говорить о группах пациентов, которым можно проводить эрадикационную терапию с точки зрения профилактики рака желудка, то очевидно, что в первую очередь нужно назвать больных гастритом. Это выраженный пангастрит, гастрит с преимущественным поражением тела желудка, выраженная атрофия.
Но если мы говорим о назначении эрадикационной терапии как профилактике рака желудка, могут учитываться и желания пациента. Например, страх заболеть раком желудка у Helicobacter pylori позитивных лиц.
И для того чтобы сделать возможным вот такую практическую профилактику рака желудка, Российская Гастроэнтерологическая Ассоциация в своих рекомендациях по диагностике и лечению инфекции Helicobacter pylori у взрослых называет хронический гастрит хеликобактерный, в том числе атрофический гастрит, как показание для проведения эрадикационной терапии.
Как проводится эрадикационная терапия, вы прекрасно знаете. На схемах сегодня остановится подробно Аркадий Александрович. И, конечно, мы начинаем со стандартной тройной терапии и говорим о том, что это схема №1 для проведения эрадикации. И конечно, нужно говорить о том, что если мы проводим эрадикационную терапию, мы должны назначать ее качественно, используя качественные препараты. Это касается и антибиотиков. В первую очередь я бы хотела акцентировать ваше внимание на кларитромицине, это основной антибиотик для стандартной тройной терапии.
И кларитромицин – конечно, с точки зрения качественного препарата для эрадикации надо упомянуть Клацид компании «Эбботт», который, в общем-то, в лучшую сторону отличается от многих препаратов, которые представлены на современном рынке, с точки зрения, например, содержания примесей или содержания действующего вещества.
Ну и, конечно, базисные препараты для проведения эрадикации – это ингибиторы протонной помпы. И я уже говорила сегодня о том, что современные ингибиторы протонной помпы, в том числе рабепразол, благодаря мощному антикислотному эффекту являются более выигрышными для проведения эрадикационной терапии. Вы видите, что у рабепразола более мощно выражен кислотоподавляющий эффект, время с pH>4 при назначении уже первой дозы этого ингибитора протонной помпы отличается в выигрышную сторону по сравнению с другими препаратами.
Конечно, невозможно не сказать о том, что с точки зрения процента эрадикации схемы, основанные на современных ингибиторах протонной помпы, тоже дают определенное преимущество. Мы видим, что по сравнению с другими ингибиторами протонной помпы – лансопразолом, пантопразолом, омепразолом – схемы, основанные на рабепразоле, дают более высокий процент эрадикации.
Почему? Потому что вы видите уже не результаты первого дня приема ингибитора протонной помпы, а вы видите результаты метаанализа 57 исследований, где доказано, что процент времени с pH>4 при курсовом приеме стандартной дозы рабепразола действительно очень высокий. И вы видите данные метаанализа, которые конкретно сравнивают уже эффективность эрадикационной терапии. Здесь показано, что схемы на основе рабепразола обладают более высоким процентом эрадикации – 80,5%, по сравнению с более старыми ингибиторами протонной помпы (омепразол, лансопразол, пантопразол) как основе схемы эрадикации.
И в завершение мне, конечно, хочется обратить ваше внимание на возможности применения в эрадикационной терапии нового ингибитора протонной помпы – это хорошо известный нам рабепразол с новым торговым названием, препарат ОнТайм. Это воспроизведенный рабепразол с доказанной высокой биоэквивалентностью. Благодарю за внимание.
Источник
Рецидив рака желудка — это возобновление роста опухоли после проведённого лечения и клинического выздоровления. К сожалению, даже после радикальной операции, которая была выполнена с соблюдением всех принципов абластики и антибластики, процент возврата опухоли достаточно велик. Поэтому пациентам, оперированным по поводу онкологических новообразований желудка, необходимо чётко соблюдать рекомендации врача и регулярно проходить контрольные обследования.
Общая информация
Рак желудка занимает лидирующие места в структуре онкологической заболеваемости и смертности. Чаще летальные исходы связаны именно с рецидивом заболевания (около 75%). По данным ряда исследователей, после проведённых радикальных операций по поводу злокачественных опухолей дистального отдела желудка, опухолевый очаг повторно диагностируется у 30-50% пациентов. Повторное новообразование чаще локализуется в культе органа или регионарных лимфоузлах.
Причины развития рецидива рака желудка
К рецидиву рака в ложе опухоли, культе желудка, зоне анастомоза и в регионарных лимфоузлах часто приводит так называемая «скрытая» микродиссеминация злокачественных клеток.
Высока вероятность возникновения повторной опухоли при:
- низкой дифференцировке новообразования;
- большом размере опухоли;
- глубокой инвазии в стенку желудка;
- прохождении линии резекции в зоне опухоли;
- поражении регионарных лимфатических узлов (чем больше лимфоузлов имеют метастазы, тем хуже прогноз).
Значительно снижается риск рецидива при выполнении операции в условиях профильной клиники. Если врач знает и применяет принципы хирургического лечения онкологических процессов, а также применяет современные протоколы лечения, вероятность того, что рак появится снова, значительно уменьшается.
Факторы риска
Рецидивы рака преимущественно возникают при 3-4 стадиях заболевания. Раком культи оперированного желудка чаще страдают пациенты, у которых:
- в процессе оперативного вмешательства была изменена стадия болезни «в большую сторону»;
- после морфологического изучения удалённой опухоли, её гистотип оказался «хуже», чем изначальный вариант (низкая дифференцировка, глубокая степень инвазии в оболочку желудка, диффузно-инфильтративная форма);
- было прорастание опухоли в пищевод.
Нередко рак культи возникает после хирургических вмешательств по поводу доброкачественных новообразований желудка. После классических операций (Б-1, Б-2) создаются благоприятные условия для развития дуоденогастрального рефлюкса. Секрет двенадцатиперстной кишки, содержащий панкреатический сок и желчь, раздражает слизистую желудка, приводя к появлению метаплазии и дисплазии.
В целом, факторы риска для рецидива рака желудка выделяют те же, что для первичных новообразований. К ним относится неправильное питание, курение, злоупотребление спиртными напитками, малоподвижный образ жизни, иммунодефицит и т.д. Большое значение для развития рака желудка имеет инфицирование бактерией Helicobacter pylori, а также наследственный фактор.
Виды рецидива
Клиницисты различают два типа рецидивов рака желудка по времени их возникновения:
- ранний — появляется в ближайшие 2 года после удаления первичной опухоли;
- поздний — развивается позже 2 лет от выполнения радикальной операции.
В большинстве случаев рецидивы случаются в первые 24 месяца после хирургического лечения. Однако выявление повторных раковых опухолей возможно спустя 5 и более лет.
В практике выделяют следующую локализацию рецидивов:
- местный, когда поражена культя желудка, область анастомоза;
- регионарный — наблюдается при рецидиве аденокарциномы в близлежащие лимфатические узлы;
- канцероматоз — рак распространяется по брюшине;
- отдалённые очаги — метастазы во внутренние органы и структуры организма.
Если стадия опухоли Т1-2, то частота региональных рецидивов не превышает 45%, при Т3-4 показатель будет не выше 20%. Как правило, повторные опухоли желудка отличаются более сильной биологической активностью, склонностью к инфильтративному росту и высокой степенью инвазивности. Они часто прорастают в соседние ткани и органы — поджелудочную железу, печень, брюшные сосуды и т. д. При рецидиве рака наблюдается более быстрое прогрессирование.
Симптомы рецидива рака желудка
При рецидиве рака желудка симптоматика во многом будет схожа с проявлениями первичной опухоли. В редких случаях признаки болезни могут отсутствовать. Среди частых клинических симптомов рецидивирующего рака желудка выделяют:
- диспепсические жалобы;
- боли различной интенсивности и характера в области эпигастрия;
- увеличение размеров живота (асцит);
- желудочное кровотечение;
- астенический синдром;
- незначительное повышение температуры тела до субфебрильных значений;
- изменение пищевых пристрастий;
- симптомы, связанные с метастатическим поражением других органов и тканей.
Часто при рецидиве злокачественных новообразований желудка у пациента резко изменяется эмоциональный фон. Он становится равнодушным к происходящему, замыкается в себе, может испытывать сильную депрессию.
Диагностика
После завершения лечения необходимо проходить контрольное обследование каждые три месяца в первый год, каждые 6 месяцев во второй год и далее — ежегодно. По показаниям врач может назначить дополнительные консультации. При поздних рецидивах нередко случаются диагностические ошибки, поэтому большое значение имеет верный алгоритм действий.
Для обнаружения повторных образований желудка применяются:
- тест на специфические маркеры при раке (РЭА, СА19-9, СА72-4 и SСС);
- лабораторные анализы;
- рентгенологические методики;
- эндоскопическое исследование оперированного желудка — хорошо видна локализация опухоли, степень её распространения, можно взять материал для гистологического изучения.
Для выявления метастазов рецидивирующего рака желудка могут быть назначены дополнительные диагностические методы, такие как УЗИ внутренних органов брюшной полости, рентгенография костей, сонография лимфатических узлов и т. д.
Лечение рецидива рака желудка
Основным радикальным вмешательством по поводу местного рецидива рака желудка считается экстирпация (полное удаление) оставшейся части органа со всеми лимфатическими узлами. Вторым этапом хирург создаёт пищеводно-кишечный анастомоз. Повторная резекция желудка проводится редко и при наличии чётких показаний, так как не является достаточно радикальным методом при рецидиве.
Если технически невозможно провести операцию при раке культи или патология приняла диссеминированный характер, больному может быть назначена химиотерапия или паллиативное облучение. Выбор тактики будет обусловлен распространённостью злокачественного процесса и состоянием пациента.
Прогноз при рецидиве рака желудка
Рецидив рака желудка характеризуется более плохим прогнозом, чем первичный злокачественный процесс. 5-летняя выживаемость в разных возрастных группах не превышает 30%. Повторный рак характеризуется выраженной агрессивностью и часто плохо поддаётся лечению. Рецидивы могут существенно отличаться по всем характеристикам от первоначального новообразования.
Лучшим прогноз выживаемости будет при выполнении хирургических повторных вмешательств. При отсутствии радикального лечения, шансы достигнуть ремиссии при рецидивирующем раке желудка очень малы.
Цены на лечение
При рецидиве стоимость лечения рака желудка зависит от множества факторов. Основным критерием является выбор метода (оперативный, химиотерапия или облучение). Цена хирургического вмешательства при рецидиве рака в среднем варьирует от 78 000 до 130 000 рублей.
Несмотря на то, что рецидив рака желудка — это неблагоприятный признак, вовремя проведенное адекватное лечение позволяет значительно продлить жизнь пациента, улучшить ее качество, а в ряде случаев и полностью излечиться от заболевания.
Источник
Рак желудка – злокачественная опухоль, которая развивается из клеток слизистой оболочки желудка. По распространенности он занимает пятое место среди всех видов рака. Как правило, болеют люди старше 40 лет. Основной метод лечения – хирургический, удаление всего желудка или его пораженной части.
Причины рака желудка
Точные причины рака желудка неизвестны. В слизистой оболочке органа возникают мутации ДНК, и получаются «неправильные» клетки, которые могут приобрести способность к неконтролируемому росту. Почему это происходит — не совсем понятно. Зато хорошо изучены факторы риска — условия, которые повышают риск рака желудка.
Наследственность и рак желудка
Некоторые люди носят в себе «бомбу замедленного действия», спрятанную в генах. Иногда даже не одну. Это подтверждается некоторыми фактами:
- Если у близкого родственника (родители, братья, сестры, дети) человека диагностирован рак желудка, его риски повышены примерно на 20%.
- Мужчины болеют чаще, чем женщины. Сложно сказать, с чем конкретно это связано, но можно предположить, что замешана разница между мужскими и женскими генами.
- Японцы, которые мигрировали в США, болеют раком желудка реже соотечественников, но чаще, чем «коренные» американцы. Это говорит о том, что дело не только в характере питания, но и в наследственности. Главный подозреваемый — ген под названием RNF43.
- Карцинома — самый распространенный тип рака желудка — чаще встречается у людей с группой крови A (II), которую они, конечно же, получили вместе с генами.
- Риски повышены при некоторых наследственных заболеваниях: злокачественной анемии (в 3-6 раз), гипогаммаглобулинемии, неполипозном раке толстой кишки.
- Заболеваемость раком желудка повышается после 70 лет: считается, что это происходит из-за того, что с возрастом в клетках тела накапливаются нежелательные мутации.
Рак желудка и характер питания
Роль питания в возникновении злокачественных опухолей желудка изучена хорошо. Риски повышает большое количество соли, крахмала, нитратов, некоторых углеводов. Чаще болеют люди, которые едят много соленых, копченых, маринованных продуктов, мало овощей и фруктов.

Рак желудка и вредные привычки
Курение повышает риск рака желудка примерно вдвое. Ученые в Великобритании считают, что примерно каждый пятый случай связан именно с курением. Когда человек вдыхает табачный дым, часть его попадает в желудок, и содержащиеся в нем вредные вещества повреждают клетки слизистой оболочки. Риски тем выше, чем больше стаж курильщика и ежедневное количество сигарет. Алкоголь тоже в списке подозреваемых, но прямых доказательств пока нет.
Хеликобактер пилори (H. Pylori) и рак желудка
H. Pylori — бактерия, которая способна вызывать язвенную болезнь и хронический атрофический гастрит. В настоящее время она считается важным фактором развития рака желудка. При хеликобактерной инфекции вероятность возникновения злокачественной опухоли в желудке повышается в 4 раза. В половине удаленных опухолей обнаруживают этого возбудителя.
Другие факторы риска
- Язвенная болезнь. Данные исследований по этому поводу противоречивы. Если язва находится в теле желудка, риск рака повышается почти в 2 раза. При язве нижнего отдела риски, видимо, не повышаются.
- Аденоматозные полипы слизистой оболочки.
- Семейный аденоматозный полипоз – заболевание, вызванное мутацией в гене APC и приводящее к возникновению множества полипов в желудке, кишечнике. При этом незначительно повышается риск рака.
- Перенесенные на желудке операции повышают риск рака в 2,5 раза. Это происходит из-за того, что желудок производит меньше соляной кислоты, и в нем активнее размножаются бактерии, продуцирующие нитриты, происходит обратный заброс желчи из тонкой кишки. Обычно злокачественные опухоли возникают спустя 10-15 лет после хирургического вмешательства.
- Социальное и материальное положение: риск увеличивается при низком уровне доходов, проживании в перенаселенной квартире, без удобств, в неблагоприятном районе.
- Другие онкологические заболевания: рак пищевода, простаты, мочевого пузыря, молочных желез, яичников, яичек.
- Болезнь Менетрие (гипертрофическая гастропатия) характеризуется разрастанием слизистой оболочки желудка, появлением в ней складок и снижением продукции соляной кислоты. Патология встречается редко, поэтому неизвестно, как часто она приводит к раку желудка.
- В группе повышенного риска работники угольной, металлургической и резиновой промышленности.
- Иммунодефицит повышает вероятность развития рака, лимфомы желудка.
Классификация рака желудка: каким он бывает?
Злокачественные опухоли желудка, согласно Международной гистологической классификации ВОЗ, делят на 11 типов, в зависимости от того, из каких клеток они происходят. Преобладает рак из железистых клеток, которые выстилают слизистую оболочку и вырабатывают слизь — аденокарцинома. Он составляет 90-95% всех случаев. Также встречаются опухоли из иммунных (лимфома), гормонпродуцирующих (карциноид) клеток, из нервной ткани.
Одна из старейших классификаций делит злокачественные опухоли желудка на 3 типа:
- Кишечный. Как следует из названия, в окружении опухоли имеется кишечная метаплазия, то есть слизистая оболочка желудка становится похожа на слизистую кишечника. Этот тип рака чаще встречается у пожилых людей, отличается более благоприятным прогнозом. Это типично «японский» тип рака.
- Диффузный. Опухолевые клетки расползаются по стенке желудка, они окружены нормальной слизистой оболочкой.
- Смешанный.
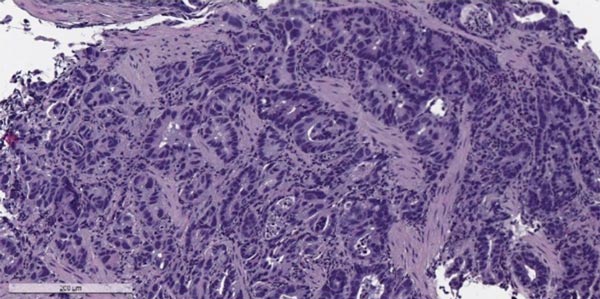
Аденокарцинома желудка
Стадии рака желудка
Рак желудка делят на ранний (начальный) и распространенный. При раннем опухоль не прорастает глубже слизистой оболочки и подслизистой основы. Такие опухоли проще удалить (в том числе эндоскопическим путем), при них лучше прогноз. Также используют классификацию TNM, которая учитывает размеры и прорастание в разные ткани первичной опухоли (T), метастазы в регионарных (близлежащих) лимфатических узлах (N), отдаленные метастазы (M).
Классификация в зависимости от состояния первичной опухоли (T):
- Tx – первичную опухоль невозможно оценить;
- T0 – первичная опухоль не обнаруживается;
- T1 – тяжелая дисплазия клеток слизистой оболочки, опухоль находится в поверхностном слое слизистой оболочки (“рак на месте”);
- T2 – опухоль проросла в мышечный слой стенки органа;
- T3 – рак достиг серозной (наружной) оболочки желудка, но не пророс в нее;
- T4 – опухоль проросла в серозную оболочку (T4a), в соседние структуры (T4b).
Классификация в зависимости от наличия поражения в регионарных лимфатических узлах:
- Nx – невозможно оценить метастазы в лимфатических узлах;
- N0 – метастазы в регионарных лимфоузлах не обнаружены;
- N1 – поражены 1-2 лимфоузла;
- N2 – опухолевые клетки распространились в 3-6 лимфоузлов;
- N3 – метастазы в 7-15 (N3a) или в 16 и более (N3b) лимфоузлах.
Классификация в зависимости от наличия отдаленных метастазов:
- M0 – отдаленные метастазы не обнаружены;
- M1 – обнаружены отдаленные метастазы.
Аденокарциному делят на 4 стадии:
- I стадия (T1M0N0 – стадия Ia; T1N1M0, T2N0M0 – стадия Ib). Опухоль находится в пределах слизистой оболочки и подслизистой основы, не прорастает вглубь стенки желудка. Иногда раковые клетки обнаруживают в близлежащих лимфатических узлах.
- II стадия (T1N2M0, T2N1M0, T3N0M0 – стадия IIa; T1N3aM0, T2N2M0, T3N1M0, T4aN0M0 – стадия IIb). Опухоль прорастает в мышечный слой стенки желудка и распространяется в лимфатические узлы.
- III стадия (T2N3aN0, T3N2M0, T4aN1M0, T4aN2M0 – стадия IIIa; T1N3bM0, T2N3bM0, T3N3aM0, T4aN3aM0, T4bN1M0 – стадия IIIb; T3N3bM0, T4aN3bM0, T4bN3aM0 – стадия IIIc). Рак пророс через всю стенку желудка и, возможно, распространился на соседние органы, успел сильнее поразить близлежащие лимфатические узлы.
- IV стадия (любые T и N, M1). Есть отдаленные метастазы.
Метастазы рака желудка
Раковые клетки могут отрываться от материнской опухоли и мигрировать в другие части тела различными путями:
- С током лимфы они могут попасть в лимфатические узлы брюшной полости, а из них — в лимфоузлы надключичной области — метастаз Вирхова. Метастаз в лимфоузлы, окружающие прямую кишку, называют метастазом Шницлера.
- С током крови раковые клетки чаще всего распространяются в печень, реже — в легкие.
- Также раковые клетки могут рассеиваться по брюшной полости. Если они оседают на яичниках, образуется метастаз Крукенберга, в пупке — метастаз сестры Марии Джозеф.Редко при раке желудка обнаруживают метастазы в головном мозге, костях.
Симптомы: как проявляется рак желудка?
На ранних стадиях рак желудка либо не имеет симптомов вообще, либо маскируется под другие заболевания: гастрит, обострение язвенной болезни. Ухудшение аппетита и боли под ложечкой редко заставляют людей сразу же подозревать онкозаболевание и бежать в больницу. Обычно ограничиваются диетой и приемом разрекламированных таблеток «от желудка». Если человек уже страдает язвенной болезнью, он может воспринять первые признаки рака желудка как очередное обострение язвы. И уже позже, когда диагностировано онкологическое заболевание, больной вспоминает, что проявления были «не такими, как всегда».
Существует так называемый «синдром малых признаков» — его сформулировал один из основоположников советской онкологии, Александр Иванович Савицкий. Если беспокоят похожие симптомы — это повод сходить к врачу и провериться:
- Необъяснимая слабость и повышенная утомляемость.
- Плохой аппетит.
- Снижение работоспособности.
- Потеря веса.
- «Желудочный дискомфорт»: неприятные ощущения, из-за которых даже любимая еда больше не радует.
В дальнейшем нарастают более яркие, «кричащие» признаки. Они зависят от того, в какой части органа находится опухоль:
- Дисфагия. Возникает, если новообразование сдавливает место перехода желудка в пищевод. Сначала становится сложно глотать твердую пищу, затем и жидкую.
- Рвота недавно съеденной пищей. Характерна для опухолей в нижней части желудка, в месте перехода в двенадцатиперстную кишку.
- Стойкая изжога.
- Постоянные боли в области желудка, которые отдают в спину. Они не проходят ни днем, ни ночью.
- Потеря веса.
- Увеличение живота. Возникает из-за асцита — скопления жидкости в брюшной полости.
- Под ложечкой можно почувствовать и нащупать жесткое выпирающее образование. Это — опухоль, которая срослась с передней брюшной стенкой.
Со временем в опухоли начинаются процессы изъязвления и распада, развивается желудочное кровотечение. Проявляется оно в виде черного дегтеобразного стула, рвоты, которая выглядит как «кофейная гуща» или содержит примеси алой крови. Если человек теряет много крови, он становится бледным, возникает слабость, головокружение. У некоторых людей рак диагностируется, когда их приводят в клинику в таком состоянии на машине «Скорой помощи».
Как вовремя диагностировать заболевание? Что такое скрининг, и почему он важен?
Статистика говорит о том, что в 75% случаев рак желудка диагностируют уже на распространенной стадии, когда опухоль успевает прорасти в соседние ткани, дать метастазы. Лечить таких больных сложно, прогноз, как правило, неблагоприятный. Обычно выраженные симптомы говорят о том, что рак уже успел распространиться по организму.
Как проверить желудок на рак: на ранних стадиях помогает скрининг — регулярные обследования людей, которые не испытывают никаких симптомов. В качестве скринингового исследования применяют гастроскопию — эндоскопическое исследование, во время которого в желудок вводят гибкую трубку с миниатюрной видеокамерой и лампочкой на конце. Насколько эффективна гастроскопия? Лучше всего это демонстрирует японский опыт. Распространенность рака желудка в Японии очень высока, а смертность от него одна из самых низких в мире. Достичь этого удалось благодаря внедрению массового скрининга.
В Европейской онкологической клинике существуют специальные скрининговые программы, которые помогают вовремя диагностировать разные онкологические заболевания. Посетите врача, узнайте о своих рисках и получите индивидуальные рекомендации по поводу скрининга.
Какие методы диагностики может назначить врач?
Помимо гастроскопии, программа диагностики рака желудка может включать:
- Рентгенографию, перед которой пациенту дают выпить контрастный раствор. При этом контуры желудка хорошо видны на снимках.
- Компьютерную томографию, позитронно-эмиссионную томографию.
- Диагностическую лапароскопию. Это операция, во время которой в живот пациента через отверстия вводят лапароскоп с миниатюрной видеокамерой и специальные инструменты. Процедура помогает оценить, как далеко за пределы желудка успел распространиться процесс.
- Биопсию. Врач получает образец подозрительной ткани и отправляет в лабораторию для изучения под микроскопом. Этот метод диагностики помогает максимально точно диагностировать онкологическое заболевание и установить тип рака. Биопсию можно провести во время гастроскопии, хирургического вмешательства.
Современные принципы лечения рака желудка
Основной метод лечения рака желудка — хирургический. Объем операции зависит от того, на какой стадии обнаружена опухоль. Если она не успела распространиться вглубь стенки органа, проводят эндоскопическую резекцию — удаление пораженного участка при помощи инструмента, введенного через рот, как во время гастроскопии.
При субтотальной гастрэктомии удаляют часть органа, пораженную опухолевым процессом. На более поздних стадиях орган приходится удалять целиком вместе с окружающими тканями. При этом пищевод соединяют с тонкой кишкой. Если лимфатические узлы в брюшной полости поражены метастазами, их также нужно удалить.
В запущенных случаях, когда излечение невозможно, проводят паллиативную операцию. Хирург удаляет пораженную часть желудка, чтобы облегчить состояние пациента.
Лучевая терапия при раке желудка бывает:
- неоадъювантной — проводится перед операцией, чтобы уменьшить размеры опухоли и облегчить её удаление;
- адъювантной — чтобы уничтожить раковые клетки, которые остались в организме после операции.
Наиболее распространенные побочные эффекты лучевой терапии при облучении области живота: тошнота, нарушение пищеварения, диарея.
Химиотерапия также бывает адъювантной и неоадъювантной. Часто её сочетают с лучевой терапией. Химиолучевая терапия может стать основным методом лечения при метастатическом раке на поздних стадиях, когда прогноз неблагоприятный, но есть возможность облегчить симптомы и продлить жизнь больного.
В некоторых случаях эффективны таргетные препараты: трастузумаб, рамуцирумаб, иматиниб, сунитиниб, регорафениб. Но они подходят лишь в тех случаях, когда опухолевые клетки обладают определенными молекулярно-генетическими свойствами.
Какой прогноз при раке желудка?
Прогноз при раке желудка зависит от стадии опухоли, на которой был установлен диагноз и начато лечение. Шансы на стойкую ремиссию наиболее высоки, если опухоль не проросла за пределы слизистой оболочки и подслизистой основы. При метастазах прогноз, как правило, неблагоприятен.
В онкологии существует такой показатель, как пятилетняя выживаемость. Он показывает, какой процент больных остаются живы в течение 5-ти лет. Срок достаточно большой, в определенном смысле его можно приравнять к выздоровлению. Пятилетняя выживаемость при разных стадиях рака желудка составляет:
- I стадия — 57-71%;
- II стадия — 33-46%;
- III стадия — 9-20%;
- IV стадия — 4%.
Некоторые цифры и факты:
- Эксперты Всемирной организации здравоохранения (ВОЗ) утверждают, что ежегодно от рака желудка во всем мире погибают 754 000 людей.
- В XXI веке распространенность заболевания снижается, но в разных странах неодинаково. Так, на одного больного из Великобритании приходится двое из России и трое из Японии.
- По распространенности среди прочих онкозаболеваний рак желудка занимает пятое место, но среди причин смерти — третье.
- Одна из лидирующих стран по распространенности рака – Япония, во многом за счет характера питания.
В Европейской онкологической клинике применяются наиболее современные методы лечения рака желудка и других онкологических заболеваний. Даже если прогноз неблагоприятен, это не означает, что больному ничем нельзя помочь. Наши врачи знают, как облегчить симптомы, обеспечить приемлемое качество жизни, продлить жизнь
Цены на лечение рака желудка на 1-4 стадиях в Европейской онкологической клинике
- Консультация онколога — 5100 руб.
- Лечение рака желудка — от 60000 руб.
- Проведение внутриплевральной химиотерапии (инфузия, без стоимости лекарственных препаратов) — 21900 руб.
- Проведение иммунотерапии (без стоимости лекарственных препаратов) — 17200 руб.
