Передается ли рак желудка по наследств
Наследственный рак желудка — это разновидность злокачественной опухоли, которая развивается вследствие генетической мутации. На начальных этапах заболевание проявляется снижением массы тела, извращением вкуса, дискомфортом в эпигастрии. При прогрессировании процесса беспокоят постоянные боли в животе, нарушения питания, признаки тяжелой анемии. Диагностика включает проведение ЭФГДС с биопсией, рентгенографии, УЗИ. Для подтверждения наследственного характера рака показано генетическое тестирование. Радикальное лечение предполагает тотальную гастрэктомию с последующей химиотерапией.
Общие сведения
В России ежегодно обнаруживают 49 тысяч новых случаев рака желудка, что составляет 11% от всех злокачественных новообразований. Около 5-10% пациентов имеют отягощенный семейный онкологический анамнез. Распространенность наследственного вида опухоли одинакова у мужчин и женщин. Манифестация рака происходит преимущественно у молодых людей — средний возраст заболевших составляет 38 лет. Наиболее ранний случай болезни зарегистрирован в 16 лет, самый поздний — в 82 года.

Наследственный рак желудка
Причины
Возникновение наследственного диффузного рака желудка (ДРЖ) обусловлено мутацией в гене CDH1. Он кодирует молекулу Е-кадгерина — белка, который обеспечивает прочность межклеточных контактов. Генетики выявили более 80 различных вариантов мутации этого гена, каждая из которых передается по наследству и представляет высокий риск развития злокачественной неоплазии. Рак желудка возникает у 80% людей, которые имеют дефект гена CDH1.
Факторы риска
Вероятность появления рака желудка повышается при наличии поведенческих факторов риска: употреблении в пищу большого количества крахмалистых продуктов и животных жиров, овощей, содержащих нитриты и нитраты. Раздражающее действие сигаретных смол и алкоголя вызывает эрозивные изменения в гастральной слизистой, которые способствуют злокачественной трансформации клеток. Манифестация наследственного онкопроцесса зачастую спровоцирована хроническим атрофическим гастритом, желудочными полипами.
Патогенез
В норме ген CDH1 действует как природный супрессор опухолевого роста. Он предотвращает появление миссенс-мутаций и делеций, эпигенетических нарушений. При неправильном строении гена создаются благоприятные условия для опухолевой трансформации клеток слизистой оболочки органа. В дальнейшем происходят симметричные и асимметричные мутации клеток-предшественников, что лежит в основе малигнизации.
При отсутствии белка Е-кадгерина гастральный эпителий теряет свои адгезивные свойства, в результате чего нарушаются межэпителиальные соединения. Изменяется апикально-базальная полярность клеток, наблюдается неравномерное клеточное деление. При дальнейшем прогрессировании патологии начинается инвазивный рост наследственного рака в подслизистый и мышечный слои желудка, лимфогенное и контактное метастазирование.
Классификация
В онкологии применяют стандартный метод классификации новообразований желудка по системе TNM. Символ T обозначает глубину инвазии первичного очага, N — злокачественное поражение регионарных лимфоузлов, M — наличие или отсутствие отдаленных метастазов. В клинической практике врачи-онкологи широко используют классификацию наследственного рака желудка, которая включает 4 стадии:
- I стадия. Предполагает распространение опухолевых клеток не глубже мышечной пластинки слизистой оболочки и поражение 1-2 лимфатических узлов.
- II стадия. Характеризуется инвазией рака вглубь до висцеральной брюшины включительно с незначительным поражением лимфоузлов. К этой стадии относят множественные метастазы в лимфатические узлы при неглубоком распространении злокачественного объемного образования.
- III стадия. Наблюдается глубокая инвазия злокачественных клеток в желудочную стенку и соседние органы в сочетании с множественным поражением лимфоузлов.
- IV стадия. Устанавливается при любой распространенности процесса, если обнаруживаются отдаленные метастазы.
Симптомы
Коварство наследственного рака желудка заключается в его длительном малосимптомном течении. На 1-2 стадиях заболевания у половины пациентов клинические признаки отсутствуют. Начальные проявления опухоли неспецифичны: дискомфорт и периодическая умеренная болезненность в эпигастральной области. Реже беспокоят тошнота, тяжесть в животе после еды. Боль в желудке не связана с приемом пищи или другими провоцирующими факторами, обычно она ощущается утром.
Для опухолевого поражения желудка характерно преобладание общих симптомов. Больные отмечают немотивированную слабость и повышенную утомляемость. Человек не чувствует себя отдохнувшим даже утром после ночного сна. Кожные покровы становятся бледными с сероватым оттенком. Постепенно снижается аппетит, происходит потеря веса. Характерным признаком является внезапное изменение вкусовых предпочтений, отказ от мясной пищи.
На поздних стадиях неопроцесса наблюдаются постоянная тупая или ноющая боль в эпигастрии. Появляются затруднения проглатывания твердой еды. Даже после приема небольших порций пищи симптомы усиливаются. Изредка открывается рвота «кофейной гущей» или застойным желудочным содержимым. Отсутствие аппетита и сознательные ограничения в объеме питания приводят к резкому похудению вплоть до кахексии.
Осложнения
У всех больных со временем возникает тяжелая В12-дефицитная анемия, которая обусловлена отсутствием внутреннего фактора Касла. Помимо нарушений кроветворной функции при этом состоянии присоединяются неврологические патологии: фуникулярный миелоз, расстройства вегетативной иннервации. С мутацией гена CDH1 ассоциировано еще одно заболевание — лобулярный рак груди, который встречается у 39-54% женщин с наследственной опухолью желудка.
К частым осложнениям гастрального рака относят прорастание неоплазии в соседние органы и ткани (25,6%), стеноз пилорического отдела (13,3%), сужение кардии (5,6%). Вследствие разрушения стенок кровеносных сосудов развиваются профузные желудочно-кишечные кровотечения. Запущенные формы характеризуются неблагоприятным течением. При III стадии процесса на протяжении 5 лет после постановки диагноза умирает 62% больных, при IV стадии — 95%.
Диагностика
При сборе анамнеза настораживающим считается наличие случаев злокачественных опухолей желудка у родственников первой-второй линии родства, появление симптомов в молодом и среднем возрасте. Диагностика наследственного ДРЖ не отличается от стандартных методов исследования при гастральном раке. Для подтверждения диагноза онколог должен оценить результаты нескольких диагностических методик, основными из которых являются:
- ЭФГДС. На начальных стадиях очаги опухолевого роста визуализируются в виде бледно-розовых или белесоватых ограниченных участков слизистой. Для уточнения диагноза проводится их окрашивание анилиновыми красителями. При прогрессирующей болезни выявляют глубоко прорастающую неоплазию, язвенные дефекты.
- Биопсия желудка. При гистологическом исследовании биоптатов обнаруживают характерную картину перстневидноклеточной карциномы. Врач определяет степень дифференцировки клеток, глубину прорастания опухолевого образования в структуру желудочной стенки. Дополнительно выполняют иммуногистохимический анализ для подбора химиотерапии.
- Рентгенография. Рентгенологическое исследование с пероральным контрастированием рекомендовано для визуализации всего пищеварительного тракта. Помимо локализации и размеров опухоли уточняют размеры органа, изучают его деформации и рубцовые сужения.
- Сонография. УЗИ брюшной полости показано для осмотра всех абдоминальных органов с целью поиска метастатических очагов. Для обнаружения типичных отдаленных метастазов наследственного рака назначается УЗИ малого таза, над- и подключичных лимфоузлов.
Для подтверждения или исключения генетического происхождения болезни проводится специальное тестирование. Согласно рекомендациям IGCLC — международной организации, занимающейся проблемами семейного и наследственного рака желудка, консультации генетика подлежат больные с ДРЖ в возрасте до 40 лет, семьи, в которых есть минимум 2 случая рака желудка и 1 подтвержденный ДРЖ. Тестирование гена CDH1 также применяется при сочетании диффузной опухоли и долькового рака молочной железы у одного пациента.
Лечение наследственного рака желудка
Консервативная терапия
Самостоятельное медикаментозное лечение наследственного варианта рака желудка не назначается. Химиотерапия используется как дополнение к оперативному вмешательству, чтобы увеличить вероятность полного выздоровления. По времени выполнения выделяют неадъювантную (проводимую перед операцией) и адъювантную терапию, которая осуществляется после удаления новообразования.
Хирургическое лечение
Единственный радикальный метод при выявлении наследственного рака — тотальная гастрэктомия. Полное удаление органа требуется, чтобы предотвратить рецидивы заболевания. Онкологи предпочитают выполнять D2-диссекцию блока лимфатических узлов с сохранением поджелудочной железы и селезенки. Благодаря современной модификации наложения анастомоза удается нормализовать время транзита пищи по кишечнику и частично сохранить пищеварительную функцию.
Экспериментальное лечение
Методика HIPEC — гипертермическая внутрибрюшная химиотерапия — рекомендована больным с распространенным опухолевым процессом при развитии множественного канцероматоза брюшины. Модификацией этого метода является распыление аэрозоля с химиопрепаратами под давлением (PIPAC), что способствует более глубокому проникновению лекарства в опухолевую ткань.
Прогноз и профилактика
Вероятность выздоровления и ожидаемая продолжительности жизни зависит от стадии наследственного рака и объема лечения. Проведение операции на ранних стадиях обеспечивает 5-летнюю выживаемость и хорошее качество жизни у 90% пациентов. В практической онкологии ведется разработка новых подходов к терапии, которые направлены на продление жизни больным с запущенными формами опухоли.
Активно обсуждается целесообразность проведения профилактической гастрэктомии людям, у которых выявлена характерная мутация, но признаки наследственного рака отсутствуют. Такой подход предотвращает развитие неоплазии, но операция влияет на физическое здоровье и психологический комфорт пациента. Альтернативной профилактикой является регулярный эндоскопический контроль состояния гастрального эпителия.
Источник
6 февраля 2019 г.
Просмотров: 4010
Вы наверняка не раз задавались этим вопросом, если у кого-то из ваших родственников обнаруживали онкологическое заболевание. Многие люди теряются в догадках – что делать, если бабушки и прабабушки умирали в 30-40 лет, а никакой информации об их заболеваниях нет? А если они умирали в 60 «по старости», как и все в то время, была ли это онкология? Может ли она возникнуть у меня?
Когда родственник заболевает раком, нам страшно. В какой-то мере страшно и за свое здоровье – передается ли рак по наследству? Прежде чем делать поспешные выводы и впадать в панику, давайте разберемся с этим вопросом.
Последние десятилетия ученые всего мира плотно занимаются изучением рака и даже научились лечить некоторые его виды. Важные открытия происходят и в области генетики, например, в конце прошлого года немецкие молекулярные биологи обнаружили причину примерно трети случаев развития рака. Генетикам удалось выявить причины хромотрипсиса, так называемого «хромосомного хаоса». При нем хромосомы распадаются на части, а при случайном их воссоединении клетка либо гибнет, либо становится началом раковой опухоли.
Мы в клинике «Медицина 24/7» стараемся активно применять достижения генетиков в повседневной практике: определяем предрасположенность к различным видам рака и наличие мутаций – с помощью генетических исследований. Если вы входите в группу риска – о ней мы расскажем чуть позже – вам стоит обратить внимание на эти исследования. А пока – вернемся к вопросу.
По своей сути, рак – генетическое заболевание, которое возникает вследствие поломки генома клетки. Раз за разом в клетке происходит последовательное накопление мутаций, и она постепенно приобретает свойства злокачественной – малигнизируется.

Генов, которые участвуют в поломке, несколько, и перестают работать они не одновременно.
- Гены, кодирующие системы роста и деления, называются прото-онкогенами. При их поломке клетка начинает бесконечно делиться и расти.
- Есть гены-супрессоры опухолей, отвечающие за систему восприятия сигналов от других клеток и тормозящие рост и деление. Они могут сдерживать рост клетки, а при их поломке этот механизм выключается.
- И, наконец, есть гены репарации ДНК, кодирующие белки, которые чинят ДНК. Их поломка способствуют очень быстрому накоплению мутаций в геноме клетки.
Генетическая предрасположенность к онкологии
Существует два сценария возникновения мутаций, вызывающих онкологические заболевания: ненаследственный и наследственный. Ненаследственные мутации появляются в изначально здоровых клетках. Они возникают под воздействием внешних канцерогенных факторов, например, курения или ультрафиолетового излучения. В основном рак развивается у людей в зрелом возрасте: процесс возникновения и накопления мутаций может занимать не один десяток лет.
Однако, в 5-10% случаев предопределяющую роль играет наследственность. Происходит это в том случае, когда одна из онкогенных мутаций появилась в половой клетке, которой посчастливилось стать человеком. При этом каждая из примерно 40*1012 клеток организма этого человека также будет содержать начальную мутацию. Следовательно, каждой клетке нужно будет накопить меньше мутаций, чтобы стать раковой.
Повышенный риск развития рака передается из поколения в поколение и называется наследственным опухолевым синдромом. Встречается данный синдром довольно часто – примерно у 2-4% населения.
Несмотря на то, что основную массу онкологических заболеваний вызывают случайные мутации, наследственному фактору также необходимо уделять серьезное внимание. Зная об имеющихся унаследованных мутациях, можно предотвратить развитие конкретного заболевания.
Наследственные формы есть практически у любого онкологического заболевания. Известны опухолевые синдромы, которые вызывают рак желудка, кишечника, мозга, кожи, щитовидной железы, матки и другие, менее распространённые типы опухолей. Эти же типы могут быть и ненаследственными, а спорадическими (единичными, проявляющимися от случая к случаю).
Предрасположенность к раку наследуется как Менделевский доминантный признак, иными словами, как обычный ген с различной частотой возникновения. При этом вероятность возникновения в раннем возрасте у наследственных форм выше, чем у спорадических.
Распространенные генетические исследования
Коротко расскажем вам об основных видах генетических исследований, которые показаны людям из группы риска. Все эти исследования можно провести в нашей клинике.
Определение мутации в гене BRCA
В 2013 году благодаря Анджелине Джоли весь мир активно обсуждал наследственный рак молочной железы и яичников, о мутациях в генах BRCA1 и BRCA2 теперь знают даже неспециалисты. Из-за мутаций теряются функции белков, кодируемых этими генами. В результате основной механизм репарации (восстановления) двунитевых разрывов молекулы ДНК нарушается, и возникает состояние геномной нестабильности – высокой частоты мутаций в геноме клеточной линии. Нестабильность генома является центральным фактором канцерогенеза.
Говоря простым языком, гены BRCA1/2 отвечают за восстановление повреждений ДНК, а мутации в этих генах нарушают это самое восстановление, таким образом, стабильность генетической информации теряется.
Учеными описано более тысячи различных мутаций в этих генах, многие из которых (но не все) связаны с повышенным риском возникновения онкологического заболевания.
У женщин с нарушениями в BRCA1/2 риск заболеть раком молочной железы составляет 45-87%, в то время как средняя вероятность этого заболевания – всего 5,6%. Растет вероятность развития злокачественных опухолей и в других органах: яичниках (с 1 до 35%),поджелудочной, а у мужчин – и в предстательной железе.
Генетическая предрасположенность к наследственному неполипозному колоректальному раку (синдром Линча)
Колоректальный рак – одно из самых распространенных онкологических заболеваний в мире. Около 10% населения имеет генетическую предрасположенность к нему.
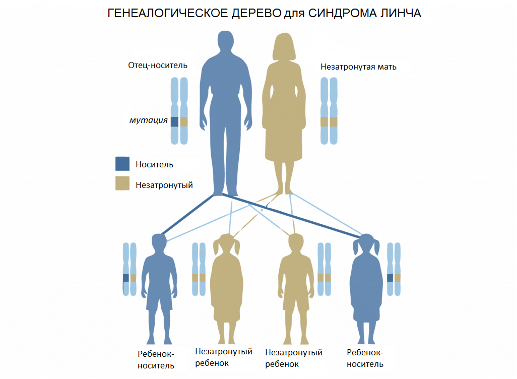
Генетический тест на синдром Линча, также известного как наследственный неполипозный колоректальный рак (НПКР),определяет заболевание с точностью 97%. Синдром Линча – наследственное заболевание, в результате которого злокачественная опухоль поражает стенки толстого кишечника. Считается, что около 5% всех случаев колоректального рака связаны с этим синдромом.
Определение мутации в гене BRaf
При наличии меланомы, опухолей щитовидной или предстательной железы, опухоли яичников или кишечника рекомендуется (а в некоторых случаях обязательно) проведение анализа на BRaf мутацию. Это исследование поможет выбрать необходимую стратегию лечения опухоли.
BRAF – это онкоген, который отвечает за кодировку белка, располагающегося в сигнальном пути Ras-Raf-MEK-MARK. Этот путь, в норме, регулирует деление клеток под контролем фактора роста и различных гормонов. Мутация в онкогене BRaf приводит к избыточному неконтролируемому разрастанию и устойчивости к апоптозу (запрограммированной смерти). Результатом является в несколько раз ускоренное размножение клеток и рост новообразования. По показаниям данного исследования специалист делает заключение о возможности использования ингибиторов BRaf, которые продемонстрировали значительное преимущество по сравнению со стандартной химиотерапией.

Методика проведения анализа
Любой генетический анализ – сложная многоэтапная процедура.
Генетический материал для анализа берут из клеток, как правило, из клеток крови. Но в последнее время лаборатории переходят на неинвазивные методы и иногда выделяют ДНК из слюны. Выделенный материал подвергается секвенции – определению последовательности мономеров при помощи химических анализаторов и реакций. Эта последовательность и является генетическим кодом. Полученный код сравнивают с эталонным и определяют, какие участки относятся к тем или иным генам. На основании их наличия, отсутствия или мутации делают заключение о результатах теста.
Сегодня в лабораториях множество методов генетического анализа, каждый из них хорош в тех или иных ситуациях:
- FISH–метод (fluorescence in situ hybridization ). В полученный от пациента биоматериал вводят специальный краситель – ДНК-пробу с флуоресцентными метками, которые способны показать хромосомные аберраций (отклонения),значимые для определения наличия и прогноза развития некоторых злокачественных процессов. Например, метод удобен при определении копий гена HER-2, важного признака при лечении рака молочной железы.
- Метод сравнительной геномной гибридизации (CGH). Метод позволяет сравнить ДНК здоровой ткани пациента и ткани опухоли. Точное сравнение дает понять, какие именно участки ДНК повреждены, а это дает инструменты для выбора целенаправленного лечения.
- Секвенирования нового поколения (NGS) – в отличие от более ранних методов секвенирования, «умеет читать» сразу несколько участков генома, поэтому успоряет процесс «чтения» генома. Применяется для определения в определенных участках генома полиморфизмов (замена нуклеотидов в цепи ДНК) и мутаций, связанных с развитием злокачественных опухолей.
За счет большого количества химических реактивов процедуры генетических исследований достаточно финансово затратные.. Мы стараемся устанавливать оптимальную стоимость всех процедур, поэтому цена на такие исследования у нас начинается от 4 800 рублей.
Группы риска
В группы риска по наследственному раку попадают люди, у которых наблюдается хотя бы один из перечисленных факторов:
- Несколько случаев одного вида рака в семье
(например, рак желудка у деда, отца и сына); - Заболевания в раннем для данного показания возрасте
(например, колоректальный рак у пациента моложе 50 лет); - Единичный случай определенного вида рака
(например, рак яичников, или трижды негативный рак молочной железы); - Рак в каждом из парных органов
(например, рак левой и правой почки); - Больше одного типа рака у родственника
(например, сочетание рака молочной железы и рака яичников); - Рак, нехарактерный для пола пациента
(например, рак молочной железы у мужчины).
Если для человека и его семьи характерен хотя бы один фактор из списка, то следует получить консультацию у врача-генетика. Он определит, есть ли медицинские показания для того, чтобы сдавать генетический тест.
Чтобы обнаружить рак на ранней стадии, носителям наследственного опухолевого синдрома следует проходить тщательный скрининг на онкологические заболевания. В некоторых случаях риск развития рака можно существенно снизить с помощью превентивных операций и лекарственной профилактики.
Для этого в клинике «Медицина 24/7» создано консультативно-диагностическое отделение. Здесь мы проводим экспресс-диагностику пациентов с подозрением на наличие онкологических заболеваний и углубленное обследование людей с уже установленным диагнозом.
Генетический «вид» раковой клетки в процессе развития изменяется и теряет свой первоначальный вид. Поэтому, чтобы использовать молекулярные особенности рака для лечения, недостаточно исследовать только наследственные мутации. Для выявления слабых мест опухоли нужно провести молекулярное тестирование образцов, полученных в результате биопсии или операции.
При проведении теста опухоль анализируется, составляется индивидуальный молекулярный паспорт. В комплексе с анализом крови, в зависимости от требуемого теста, проводится комбинацирование различных анализов на геном и белок. В результате данного теста появляется возможность назначения таргетной терапии, эффективной для каждого типа имеющейся опухоли.
Профилактика
Бытует мнение, что для определения предрасположенности к раку можно сделать простой анализ на наличие онкомаркеров – специфических веществ, которые могут быть продуктами жизнедеятельности опухоли.
Однако более половины онкологов нашей страны признают, что данный показатель неинформативен для профилактики и раннего выявления – он дает слишком высокий процент ложноположительных и ложноотрицательных результатов.
Повышение показателя может зависеть от целого ряда причин, совершенно не связанных с онкологическими заболеваниями. В то же время, есть примеры людей с онкологическими заболеваниями, у которых значения онкомаркера оставались в пределах нормы. Специалисты используют онкомаркеры как метод для отслеживания протекания уже обнаруженного заболевания, результаты которого нужно перепроверять.
Для выявления вероятности генетической наследственности в первую очередь, если вы входите в группу риска, нужно обратиться за консультацией к врачу-онкологу. Специалист, исходя из вашего анамнеза, сделает вывод о необходимости проведения тех или иных исследований.
Важно понимать, что решение о проведении какого-либо теста должен принять именно врач. Самолечение в онкологии неприемлемо. Неправильно интерпретированные результаты не только могут вызвать преждевременную панику – вы попросту можете упустить наличие развивающегося онкологического заболевания. Выявление рака на ранней стадии при наличии вовремя поставленного правильного лечения дает шанс на выздоровление.
Стоит ли паниковать?
Рак – неизбежный спутник долгоживущего организма: вероятность накопления соматической клеткой критического числа мутаций прямо пропорциональна времени жизни. То, что рак – генетическое заболевание, не значит, что оно наследственное. Он передается в 2-4% случаев. Если у вашего родственника обнаружили онкологическое заболевание – не впадайте в панику, этим вы навредите и себе, и ему. Обратитесь к врачу-онкологу. Пройдите исследования, которые он вам назначит. Лучше, если это будет специалист, который следит за прогрессом в области диагностики и лечения рака и в курсе всего, что вы сами только что узнали. Следуйте его рекомендациям и не болейте.
Источник
