Вич и рак желудка

Рак у ВИЧ-инфицированных по своему течению радикально отличается от злокачественных процессов, развивающихся на фоне нормального или чуть сниженного иммунитета. Вирус иммунодефицита помогает онкогенезу и выживанию опухолевых клеток, поддерживая в организме больного персистентный «коктейль» из инфекционных и воспалительных процессов.
Тем не менее, в последние десятилетия адекватная противовирусная терапия позволила не только улучшить результаты противоракового воздействия, но и в разы уменьшить вероятность развития злокачественного процесса у ответственного пациента.
Когда при ВИЧ появляются злокачественные опухоли
Рак и другие злокачественные опухоли развиваются при переходе ВИЧ-инфекции в позднюю стадию болезни, когда концентрация иммунных клеток устремляется к минимальной, позволяя активно и почти беспрепятственно размножаться разнообразной микрофлоре — от простейший и грибов до бактерий и вирусов.
По классификации ВОЗ это IV стадия и есть собственно СПИД, по российским критериям — IIIB фаза «с клиническими проявлениями СПИД». В США переход ВИЧ-инфекции в завершающую стадию определяют не столько по клиническим признакам, сколь по снижению числа CD4+ лимфоцитов в кубическом миллиметре с 200 до 50 клеток до появления явных симптомов.
Всё, что происходило в организме инфицированного пациента ранее, было обычной ВИЧ-инфекцией, появление рака или других опухолей, а также тяжёлых распространённых инфекций — это уже СПИД.
Благодаря лечению период от заражения вирусом иммунодефицита до последней стадии болезни растянулся почти на три десятилетия, тогда как в конце 1980-х годов занимал несколько лет.
Продолжительность жизни существенно возросла и это заслуга высококачественной терапии или коротко — ВААРТ. Без регулярного лечения ВИЧ рискует перейти в терминальную стадию за считанные годы, как было в начале «эры ВИЧ».
Какие раки развиваются при ВИЧ-инфекции
В конце ХХ века выявление определённых, практически не встречающихся при нормальном иммунитете заболеваний и злокачественных процессов, позволяло ставить диагноз ВИЧ/СПИД без сложных лабораторных исследований. Такие процессы обозначили как ассоциированные с вирусом иммунодефицита или, по-современному, СПИД-индикаторные. В этот список наряду с необычными инфекциями включены инвазивный рак шейки матки, саркома Капоши и злокачественные лимфомы, вероятность которых у инфицированного пациента возрастает в сотни раз.
Значительно чаще, но не в сотни раз, при ВИЧ-инфекции вероятно развитие плоскоклеточного рака анального канала и рака вульвы, карциномы лёгкого и злокачественных опухолей яичка, плоскоклеточного рака головы и шеи, меланомы и рака кожи.
Для большинства злокачественных процессов доказана основополагающая патогенетическая роль вирусов, в первую очередь, папилломы человека (ВПЧ) и гепатита В, С и D. Способствует раннему развитию злокачественных новообразований носительство вирусов герпеса, особенно 4 типа — вируса Эпштейна-Барр. Традиционно значимы у ВИЧ-инфицированных факторы риска злокачественного перерождения клеток бронхолегочной системы — курение и наследственная предрасположенность.
Как ВИЧ-инфекция влияет на течение рака
Однозначно — очень неблагоприятно, усугубляя скорость прогрессирования и увеличивая массив опухолевого поражения. И хотя рак у ВИЧ-инфицированного пациента возникает много раньше, чем в общей популяции, практически в молодом возрасте, пациенты не могут похвастать исходным хорошим здоровьем.
Злокачественные процессы манифестируют начало и развитие СПИД — терминальной (последней) стадии ВИЧ, когда в организме «уживается» множество генерализованных (распространённых) инфекций, каждая из которых формирует собственный комплекс разнообразных симптомов и клинических проявлений.

Как правило, в этот период обязательно возникает вирусная лихорадка, боли в мышцах и суставах, прогрессируют неврологические нарушения и изменения психики. Активизируется герпесная группа вирусов, поражающая кожу и нервные клетки, меняется продукция гормонов, доводящая до фатальной недостаточности надпочечников. Злокачественный процесс активизируется и поддерживается «разрушением» организма.
Как ВИЧ сказывается на переносимости химиотерапии
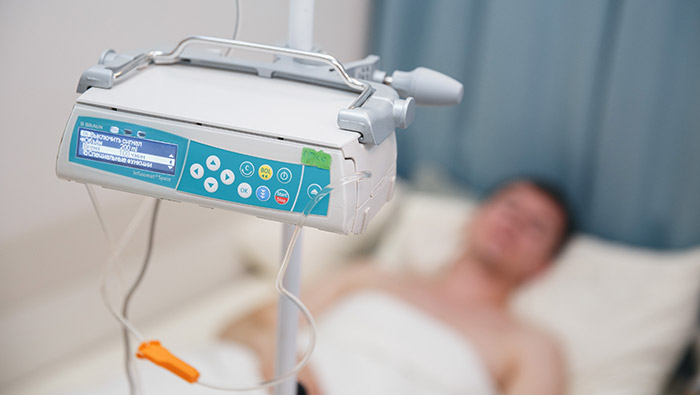
В большинстве случаев злокачественный процесс на фоне ВИЧ-инфекции течёт агрессивнее, поэтому на первом этапе требует системного лечения с использованием противоопухолевых препаратов, гарантирующих разнообразный спектр токсических реакций. При этом ни в коем случае нельзя отказываться от специфической противовирусной терапии, также изобилующей неблагоприятными проявлениями.
В итоге переносимость противоракового лечения, проводимого на фоне ВААРТ, ухудшается, а продолжительность жизни пациентов не в пример короче, чем это могло быть в отсутствии ВИЧ. При активной противоопухолевой и противовирусной терапии больше года после выявления опухоли живёт только каждый четвёртый, пятилетку — всего 19%.
Существует ещё одна серьёзная проблема — клинического изучения эффективности противоопухолевой терапии у ВИЧ-инфицированных не проводится из-за малочисленности групп пациентов и, следовательно, сомнительной достоверности результатов. Поэтому очень важно в этот тяжёлый период найти клинику и специалистов одинаково высоко компетентных в вопросах лечения ВИЧ и противораковой химиотерапии.
Как лечат рак у ВИЧ-инфицированных
В большинстве случаев терапия рака не должна отличаться от таковой у пациентов с нормальными показателями иммунитета.
При технической возможности хирургической операции ВИЧ-пациенту от неё нельзя отказываться, поскольку излечение возможно только при удалении всех очагов рака. Если для злокачественной опухоли лимфатической системы признана необходимость высокодозной химиотерапии с трансплантацией стволовых клеток, то и инфицированный вирусом пациент должен получить программное лечение. При раке шейки матки практически невозможно обойтись без лучевой терапии.
ВИЧ-компрометированному пациенту потребуется ВААРТ и гораздо более серьёзное сопроводительное лечение. Чтобы провести химиотерапию без сокращения доз и интервалов необходима индивидуальная программа реабилитационного воздействия. Кроме того, пациент должен получать множество препаратов для лечения грибковых поражений и сдерживания вирусов герпеса, разнообразные антибактериальные средства, каждое из которых имеет собственную токсичность.
Такое комплексное воздействие способна осуществить только команда врачей разных специальностей, блестяще ориентированная как в потребностях онкологического пациента, так и в возможностях организма инфицированного.
Список литературы:
- Некрасова A.В. / Онкологические заболевания у пациентов с ВИЧ-инфекцией. Взгляд клинициста // Материалы II Санкт-Петербургского форума: «Современные аспекты профилактики, диагностики и лечения ВИЧ-инфекции», 06 октября 2017 г., Санкт-Петербург
- Пивник А. В., Серегин Н. В., Пархоменко Ю. Г. с соавторами / Герминогенные опухоли у больных СПИД// Современная онкология, 2008; 2.
- Покровский В.В. / ВИЧ-инфекция и СПИД. Национальное руководство. М.: ГЭОТАР-Медиа, 2013.
- Bryant AK, Mudgway R, Huynh-Le MP, et al./ Effect of CD4 Count on Treatment Toxicity and Tumor Recurrence in Human Immunodeficiency Virus-Positive Patients With Anal Cancer // Int J Radiat Oncol Biol Phys., 2017; Sep 22.
- Вonnet F, Burty C, Lewden C, et al. / Changes in cancer mortality among HIV-infected patients: the Mortalité 2005 Survey // Clin Infect Dis 2009; 48.
- Consolidated guidelines on HIV prevention, diagnosis, treatment and care for key populations / WHO, July 2014// http: //www.who.int
- Dryden-Peterson S, Bvochora-Nsingo M, Suneja G, et al/ HIV Infection and Survival Among Women With Cervical Cancer // J Clin Oncol., 2016; Aug 29
Источник
ВИЧ-инфекция — один из факторов, который во много раз повышает вероятность развития рака. Выяснили, какие именно онкозаболевания чаще всего могут возникать при положительном ВИЧ-статусе, как их вовремя обнаружить, и на какие факторы риска еще нужно обратить внимание людям, живущим с ВИЧ.
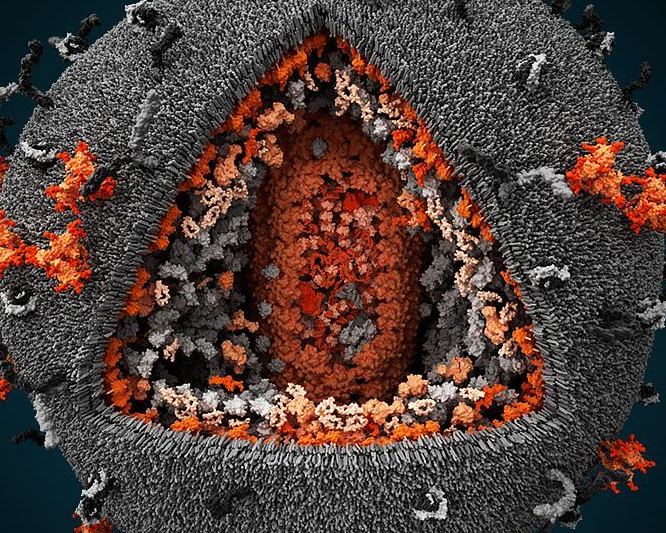
Мишень вируса
ВИЧ-инфекция вызывается рок-звездой вирусной концертной сцены, ретровирусом со сложной белковой оболочкой, которая позволяет «хозяину» мутировать и оставаться невидимым для иммунитета. Это одна из самых неуправляемых инфекций: несмотря на наличие доступной терапии, сохраняется высокий риск развития различных онкологических заболеваний.
Главная мишень вируса — CD4-Т-лимфоциты. Они передают сигнал другим клеткам, которые защищают организм от рака. В результате вмешательства вируса количество CD4-T-лимфоцитов постепенно уменьшается. Критически низкий уровень этих клеток – одна из причин отсутствия согласованной работы между звеньями иммунитета и главный механизм, приводящий к развитию СПИДа.
СПИД-индикаторные опухоли
Иммунитет человека с ВИЧ-инфекцией перестает контролировать процессы избыточного клеточного деления и злокачественной трансформации клеток. Вместе с уменьшением количества CD4-T-лимфоцитов происходит накопление раковых клеток. В результате у человека развиваются несколько видов опухолей, которые называют СПИД-индикаторными: появление такого вида рака с очень большой вероятностью означает наличие у человека СПИДа.
Однако повышается риск появления не только СПИД-индикаторных опухолей, но и тех видов рака, которые развиваются из-за потери иммунного контроля над несколькими онкогенными инфекциями: вирусом герпеса человека 8 типа (ВГЧ-8), вирусом папилломы человека (ВПЧ), вирусами гепатита В и С (ВГВ, ВГС), вирусом Эпштейна-Барр (ВЭБ) и другими.
Все эти состояния развиваются у людей с ВИЧ-инфекцией преимущественно на фоне снижения количества CD4-T-лимфоцитов до уровня менее 200 клеток/мкл (при разбросе в норме от 500 до 1100 клеток), но также могут возникать при нормальном или близком к нормальному уровню CD4-T-лимфоцитов.
Саркома Капоши
Саркома Капоши (СК) — СПИД-индикаторная опухоль, при которой происходит злокачественная трансформация клеток лимфатических и кровеносных сосудов. Риск развития СК у пациентов с ВИЧ-инфекцией увеличивается в несколько сотен раз. Различные белки ВИЧ-1 способны усиливать воспаление и нарушать регуляцию в эндотелиальных клетках. Это приводит к тому, что саркома Капоши может развиться до того, как уровень CD4-T-лимфоцитов упадет ниже 200 клеток/мкл. Еще одно обязательное условие для возникновения СК — наличие в организме вируса герпеса человека 8 типа.
Саркома Капоши развивается в виде папулы, пятна, узелка, бляшки коричневого, розового, красного или темно-красного цвета от нескольких миллиметров до нескольких сантиметров в диаметре. Обычно высыпания концентрируются на ногах, голове, шее, на слизистой оболочке — в области неба, десен, конъюнктивы.
До эры внедрения лекарств от ВИЧ — антиретровирусной терапии (АРТ) 5-летняя выживаемость (с момента диагностики опухоли) пациентов с саркомой Капоши составляла менее 10%. Применение АРТ значительно улучшило ситуацию — сейчас речь идет о 74%, — а также позволило снизить риск развития СК.
Более половины случаев СК (56%) диагностируются сейчас в локальной форме — до того, как опухоль распространится на лимфатические узлы, слизистую ЖКТ, печень, селезенку и другие органы. Прием антиретровирусной терапии помогает значительно замедлить прогрессию болезни и предотвратить распространение СК по всему организму.
К сожалению, обнаружить саркому Капоши до появления симптомов не получится
Однако, человеку с ВИЧ и его амбулаторному врачу-инфекционисту необходимо учитывать несколько факторов риска развития этой опухоли:
- Этническая принадлежность: люди еврейского или средиземноморского происхождения, а также экваториальные африканцы;
- Мужской пол;
- Иммунодефицит: Люди с уровнем CD4-клеток менее 200 кл/мкл, те, кто перенес трансплантацию органов или костного мозга или постоянно принимает глюкокортикостероиды;
- Сексуальная ориентация: мужчины, имеющие секс с мужчинами(МСМ), подвержены более высокому риску развития СК.
Опухоли, связанные с ВПЧ
К онкологическим заболеваниям, ассоциированным с вирусом папилломы человека, относятся инвазивный рак шейки матки (ИРШМ), сквамозный (чешуйчатый) рак головы/шеи, рак анального канала, вульвы и влагалища. СПИД-индикаторной из них является только ИРШМ.
Распространенность генитальной онкогенной инфекции ВПЧ среди женщин, живущих с ВИЧ, в целом выше, чем у остального населения.
Вирус папилломы человека способен к самопроизвольной элиминации — исчезновению из организма. У ВИЧ-положительных женщин этот процесс занимает больше времени, что увеличивает вероятность появления патологических изменений в шейке матки.
Продолжительный прием АРТ приводит к более низкой распространенности ВПЧ высокого риска и поражений шейки матки и даже предотвращает новые случаи ИРШМ.
Раннее начало антиретровирусной терапии, приверженность лечению обеспечивают снижение вирусной нагрузки — количества вируса в крови. Эти меры очень эффективны в отношении местного иммунитета слизистой оболочки и профилактики ИРШМ.
Скрининг ИРШМ заключается в проведении ПАП-теста и ВПЧ-теста (ПЦР). Женщины с ВИЧ-инфекцией в возрасте от 21 до 29 лет должны пройти ПАП-тест во время первичной диагностики ВИЧ, затем — через 12 месяцев, если анализ не показал патологии. Некоторые эксперты рекомендуют делать следующий ПАП-тест через 6 месяцев после первого. Если результаты трех последовательных мазков без отклонений, повторные тесты следует проводить каждые 3 года. ВПЧ-тест не рекомендуется подключать к ПАП-тесту до 30 лет — высока вероятность положительного результата, при этом оснований для активных действий нет. Лечения ВПЧ не существует, а для развития РШМ требуется, как правило, от 10 лет.
После 30 лет ПАП-тест и ВПЧ-тест проводятся совместно
Также для предотвращения ИРШМ девочкам с сопутствующей ВИЧ-инфекцией старше 9 лет и до 26 лет крайне рекомендуется вакцинация от ВПЧ-инфекции (вакцины: 2-валентный Церварикс, 4-валентный Гардасил, в Европе/США – 9-валентный Гардасил-9). Кроме ИРШМ и дисплазии вульвы и влагалища у женщин, вакцинация предотвращает развитие рака анального канала. У ВИЧ+ гетеросексуальных мужчин и МСМ риск этого вида рака возрастает в 19 раз.
О чем еще нужно знать
У пациентов с ВИЧ-инфекцией повышается риск развития:
- гепатоцеллюлярной карциномы (ГЦК), связанной с вирусами гепатита С и В (ВГВ и ВГС) — в три раза;
- рака желудка, ассоциированного с инфекцией H.pylori;
- лимфомы Ходжкина — 8-13 раз. Риск связан с сопутствующей Эпштейн-Барр-инфекцией. Важно, что повсеместное внедрение АРТ не повлияло на показатели заболеваемости лимфомой Ходжкина в популяции людей с ВИЧ.
Гепатоцеллюлярная карцинома
К факторам риска развития ГЦК у пациентов с ВИЧ относятся: цирроз печени, ожирение, диабет, возраст старше 60 лет, мужской пол.
Скрининг ГЦК проводится с помощью анализа крови на альфа-фетопротеин (АФП), который может продуцироваться раковыми клетками, или инструментальных методик диагностики — УЗИ, КТ, МРТ.
В последние годы всё чаще используется фиброскан для оценки стадии фиброза и близости к циррозу, независимому фактору риска ГЦК.
Предотвратить появление гепатоцеллюлярной карциномы можно с помощью своевременной вакцинации и ревакцинации от вирусного гепатита В и контроля вирусной нагрузки.
Неходжкинские лимфомы (НХЛ)
Несмотря на появление АРТ, НХЛ остаются актуальной проблемой для людей, длительное время живущих с ВИЧ. Хотя в большом количестве случаев неходжкинские лимфомы являются СПИД-индикаторными, они способны развиваться при нормальном уровне CD4-клеток и являются одной из наиболее частых причин смерти среди ВИЧ-положительных.
Общая выживаемость у пациентов с этим диагнозом низкая: более половины умирают в течение пяти лет от момента постановки диагноза
Одними из причин развития лимфом у ВИЧ-позитивных пациентов считаются состояние «хронического воспаления» во время какой-либо длительной инфекции (например, инфекции Helicobacter pylori, вирусного гепатита C) и аутоиммунные заболевания, предшествующие диагнозу.
Отсюда возникают факторы риска развития НХЛ при ВИЧ-инфекции:
- наличие ко-инфекции вирусными гепатитами В, C, H.pylori;
- наличие вирусной нагрузки вируса Эпштейна-Барр или цитомегаловируса;
- наличие аутоиммунных заболеваний до постановки диагноза ВИЧ-инфекция;
- наличие специфических изменений в протеинограмме до или во время ВИЧ-инфекции;
- наличие минимальной вирусной нагрузки ВИЧ, несмотря на АРТ;
- снижение CD4-Т-лимфоцитов.
К скринингу неходжкинских лимфом относятся мониторинг вирусной нагрузки ВЭБ, ВГС, ВГВ и проведение инструментальной диагностики (КТ, МРТ, УЗИ, ФГДС).
С помощью контроля факторов риска и своевременного скрининга можно не только найти опухоль на ранней стадии, но и предотвратить заболевание.
Если рак все же обнаружили, ни в коем случае нельзя прерывать антиретровирусную терапию — она проводится по жизненным показаниям, что означает высокую вероятность неблагоприятного исхода противоопухолевой терапии без сопутствующего противовирусного лечения.
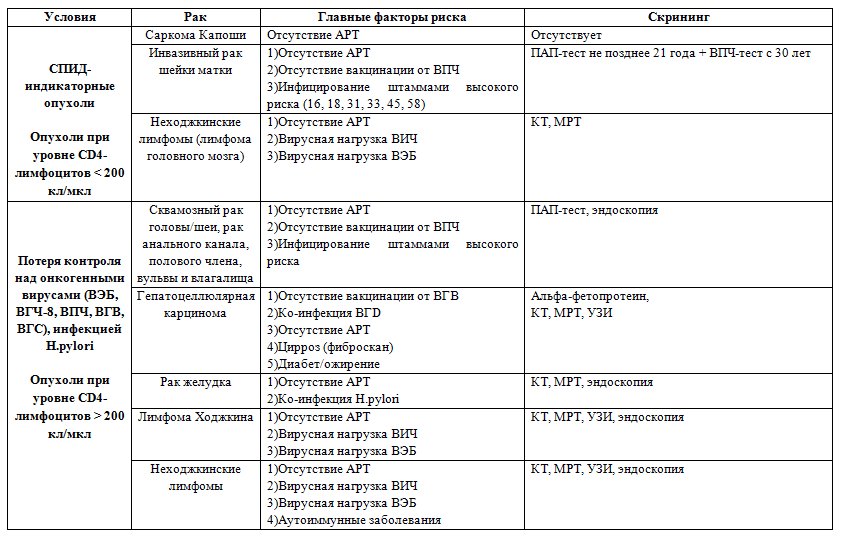
Памятка по основным факторам риска и скринингу основного перечня онкологических заболеваний, возникающих на фоне ВИЧ-инфекции
Источник
Напомним, что нет такого заболевания «рак», рак – это обобщенное название большой и разнородной группы заболеваний, у которых есть один общий знаменатель – какие-то клетки по очень различным причинам начинают бесконтрольно делиться, оказываясь там, где их быть не должно, нарушая работу органов и систем органов.
Сегодня мы знаем, что наличие ВИЧ-инфекции несет повышенные риски возникновения некоторых онкозаболеваний. Тут просто нужно сложить 2+2: некоторые виды рака связаны с вирусными поражениями, а ВИЧ-инфекция поражает наши системы защиты. Другие виды рака могут более или менее успешно контролироваться иммунной системой, а у нас именно там проблема. Все более чем очевидно. Но тут же возникает логичное предположение: а если мы начали лечение ВИЧ-инфекции очень рано, иммунная система существенно пострадать не успела, защита от вирусов не отличается от таковой у здорового человека, что же будет в таком случае?
Многие формы рака все же являются редким заболеванием, и качественное исследование в области онкологии требует длительного времени наблюдения, а также очень большого объема участников. В нашем случае – людей без ВИЧ, и это не проблема, и людей с ВИЧ, которые начали терапию рано или очень рано и многие годы поддерживали высокий уровень супрессии вируса. И вот со второй группой у нас большие проблемы. Таких людей недостаточно даже в масштабах планеты. Впрочем, некоторые ориентиры все же есть.
Департамент по делам ветеранов в США и большая группа исследователей изучили данные, полученные с 1999 по 2015 годы у 42441 человека с ВИЧ, и сравнили эти данные с показателями в группе 104712 ветеранов без ВИЧ-инфекции за тот же период. Набросок этой картины выглядит так: не подавленная вирусная нагрузка повышает риск онкозаболеваний в 2,35 раза по сравнению с людьми без ВИЧ. Своевременное начало эффективной терапии снижает риск, но он все равно почти в 2 раза выше. Более или менее своевременное начало терапии и длительное подавление еще больше снижают риски, но они все равно в 1,5 раза выше. Много? Как посмотреть… с одной стороны, в 1,5 раза выше, с другой, это то же самое, что 10 из 1000 против 15 из 1000 человек. Второе сравнение уже не выглядит столь трагичным.
Однако важно понимать, что это исследование проводилось не в России, и оно не отражает наших реалий. В реальной жизни мы крайне часто видим очень поздно выявленную ВИЧ-инфекцию, выраженный иммунодефицит, ситуации, когда саркома Капоши диагностируется в 500 раз чаще, чем без ВИЧ, неходжкинская Лимфома – более чем в 10 раз чаще, и даже рак шейки матки в 3 раза чаще. Другое ограничение этого и подобных исследований в том, что они не дают понимание потенциала и рисков тех случаев, где все сделано идеально и крайне своевременно. Есть огромные основания полагать, что в таких случаях разница рисков для людей с ВИЧ и без ВИЧ будет минимальна, а часто и вовсе будет отсутствовать.
Рассмотрим два сценария. Первый: ВИЧ-инфекция выявлена довольно рано, наблюдается высокий иммунный статус. Это грандиозный шанс снизить мешок рисков одним ударом. Начало терапии так быстро, как это возможно, без всяких остановок и перерывов позволит отодвинуть за горизонт широчайший спектр серьезных рисков, и риски онкозаболеваний тут даже не главные. Печально, но есть довольно высокая вероятность, что в СПИД Центре не оценят ваше рвение к раннему началу терапии, а то и будут откровенно не рады, учитывая большое число пациентов и весьма ограниченные возможности Центров СПИД. Не без исключений, иногда вы встретите понимание со стороны врача и даже получите более современный режим терапии, но так будет очень нечасто. Иногда разумным выбором будет самообеспечение препаратами и наблюдение в частном порядке как минимум в некотором периоде.
Второй сценарий: так вышло, что ВИЧ выявили поздно, и иммунная система прилично разрушена. Важно понимать, что вы не выбываете из игры, это не конец, и подавляющее число из тех, кто будет действовать энергично, последовательно и грамотно, прорвутся. Иммунный статус восстановится, более современные режимы терапии и грамотный менеджмент заболевания будут тому способствовать, но даже не очень современные схемы и шаблонный подход, лишь бы без грубых ошибок, все же позволят выйти из «красной зоны» и жить долго и счастливо.
И в обоих сценариях есть общий знаменатель – устранить все факторы риска, которыми можно управлять. Курение – враг номер один. Устранить гепатит С, если есть. Избавиться от Helicobacter pylori, копнуть и иные потенциальные инфекционные проблемы в желудочно-кишечном тракте и также разобраться. Есть проблемы с вирусными кожными поражениями – тоже устранять, возможно, победа придет и не сразу, но руки не опускать. Для женщины очень важно наблюдаться у грамотного современного гинеколога, который позволит свести практически к нулю риски рака шейки матки. У мужчин свои проблемы, и они тоже не должны оставаться без решений, задвигаться в долгий ящик. И так далее, полный список составить невозможно, риски и решения нужно оценивать индивидуально. Но не забываем: чем дольше мы миримся и сосуществуем с фактором риска, тем вероятнее, что риск превратится в проблему.
Выглядит, на первый взгляд, все сложно и дорого, но лишь на первый взгляд. Под руководством грамотных врачей запутанный клубок проблем легко превращается в понятный алгоритм несложных действий. Для врачей H-Clinic это обычная каждодневная работа, как и для многих наших коллег по всей стране, коих не так много, но они есть, мы их знаем и гордимся ими.
- Park LS. и др. Association of Viral Suppression With Lower AIDS-Defining and Non-AIDS-Defining Cancer Incidence in HIV-Infected Veterans: A Prospective Cohort Study. Ann Intern Med. 2018 Jun 12. PMID: 29893768.
- Hernández-Ramírez RU и др. Cancer risk in HIV-infected people in the USA from 1996 to 2012: a population-based, registry-linkage study. Lancet HIV. 2017 Nov;4(11):e495-e504. PMID: 28803888.
Партнерский материал, совместно с H-Clinic.
Источник