Иммуномодуляторы при раке желудка
Попытаться победить карциному, действуя на иммунную систему. Иммуномодуляторы при онкологии подстегивают собственную защиту организма, создавая условия для успешной борьбы с раком, но эффект будет при правильном использовании препаратов для иммунотерапии.
Иммуномодуляторы при онкологии
Восстановить развалившуюся и ослабленную защитную систему, чтобы эффективно бороться со злокачественной опухолью. Иммуномодуляторы при онкологии относятся к важному элементу противораковой терапии, но, как и с любыми другими лекарствами, необходимо всё делать правильно: любые иммунные препараты у онкопациентов – это «палка о двух концах». Они могут спасти, но могут и добить (бездумная и неадекватная иммунотерапия может стать стимулом для роста и прогрессирования злокачественного новообразования).
Иммуномодуляторы – это лекарственные препараты, оказывающие стимулирующее действие на иммунную защиту. Казалось бы, вот оно решение проблемы неэффективной терапии карцином – подстегнем иммунитет, который уничтожит раковые клетки.
По происхождению выделяют следующие варианты иммунных препаратов:
· Микробные;
· Синтетические;
· Животного происхождения (препараты тимуса);
· Цитокиновые (интелейкины, интерфероны);
· Растительные.
Можно использовать всё, что усилит иммунный надзор и простимулирует защитные клетки организма, но надо применять эффективные и безопасные препараты в нужное время. Важно помнить – иммуномодуляторы при онкологии могут помочь выжить, но могут и ускорить рост опухоли.
Правила применения иммуномодуляторов
Главное, что нужно знать: иммунотерапия – это вовсе не панацея. Пока нет ни одного лекарства, которое бы реально излечивало от рака. Иммуномодуляторы при онкологии применяются в комплексной терапии злокачественных новообразований, как один из факторов борьбы с раком. Важно помнить о следующих правилах:
Никакой универсальности: можно ни при любом виде рака, и не каждый препарат даст положительный эффект даже при одинаковых вариантах онкологии.
После стадирования: сначала диагноз и стадия рака, и только потом подбор лекарственной терапии.
Всегда должна быть цель: не просто тупо пытаться подстегивать иммунитет, а стараться действовать на определенные звенья иммунной защиты.
Не перегибать палку: лучше постепенно и медленно, строго соблюдая дозы, чем бездумно и агрессивно, полагая, что чем больше, тем лучше.
Не валить всё в кучу: лучше один препарат, чем смесь из нескольких или бездумное применение всего и сразу.
Помнить о безопасности: лучше длительно и разумно, применяя растительные средства, чем нетерпеливо и бесконтрольно, используя синтетические.
Посоветоваться с врачом: не надо думать, что все врачи-онкологи против иммуномодулирующих препаратов.
Иммунотерапия в разные периоды борьбы с онкологией
Не абы как, а всему свое время. Иммуномодуляторы при онкологии необходимо использовать тогда, когда они реально будут помогать бороться с опухолью. И всегда лучше посоветоваться с врачом-онкологом, прежде чем начинать применение каких-либо средств народной медицины на фоне проводимой комплексной терапии.
Появились жалобы, врач заподозрил рак и отправил на обследование. Пока нет диагноза, нельзя использовать никакие стимуляторы, биопрепараты и адаптогены.
Есть четкий TNM-диагноз. Выполнена операция. В послеоперационном периоде можно и нужно использовать препараты с иммуномодулирующим действием (быстрее будет восстановление, ниже риск осложнений, уменьшается вероятность рецидива и метастазирования).
После каждого курса химиотерапии. Да. Это поможет восстановить клетки крови (эритроциты, лейкоциты, тромбоциты). Снизит токсическую реакцию химиопрепаратов. Защитит от микробных и вирусных инфекций. И быстрее вернет онкопациента к нормальному ритму жизни. Между курсами ХТ можно применять сильнодействующие иммуностимуляторы (например, цитокиновые или синтетические).
На фоне ремиссии. Обязательно и постоянно. Иммуномодуляторы при онкологии могут стать реальной профилактикой возникновения поздних рецидивов. Поддержка иммунного надзора предотвратит выход из анабиоза спящих раковых клеток. Растительные иммуномодуляторы в постоянном режиме у онковыздоравливающего пациента – это безопасно, эффективно и разумно.
Ранее в Дзен-канале «Жить – онкология от А до Я» уже были статьи о растительных адаптогенах, аконите, болиголове, чаге, чистотеле и прополисе.
Статья опубликована на сайте parashistay.ru
Источник
Величайшим достижением современной онкологии в лечении рака за рубежом является разработка и внедрение в клиническую практику различных препаратов, способствующих созданию противоракового иммунитета. Эти лекарства имеют биологическое происхождение, они не токсичны, не вызывают побочных эффектов и угнетения различных функций организма больного, как химиопрепараты. Научной базой для создания такого метода лечения являются открытия в области иммунологии, в частности, у онкологических больных.
Содержание:
- Препараты иммунотерапии в современной онкологии
- Интересные исторические факты иммунотерапии в онкологии
- Механизм воздействия и основные группы препаратов иммунотерапии
- Препараты иммунотерапии для разных видов рака
- Где можно пройти лечение рака иммунопрепаратами
Препараты иммунотерапии в современной онкологии
Установлено, что при злокачественных опухолях в организме пациентов всегда имеет место снижение его защитных свойств, то есть иммунитета. Далее, учеными, исследующими иммунологию рака в крупнейших онкологических центрах мира, было обнаружено, что потенциальные раковые клетки (незрелые клетки различных тканей) ежедневно образуются в больших количествах у каждого человека. Теоретически это создает такую ситуацию, что каждый человек ежедневно рискует заболеть 6-8 видами рака. Но у большинства людей этого не случается по той причине, что постоянно срабатывает иммунная система и обезвреживает эти аномальные клетки, воспринимая их как чужеродные, и рак развивается именно тогда, когда защитная функция организма недостаточна.
Это и легло в основу идеи создания препаратов, которые могли бы естественным образом воздействовать на злокачественные клетки – как профилактически, не давая возможности развиться опухоли, так и с целью воздействия на уже имеющуюся раковую опухоль. Сегодня арсенал таких препаратов довольно широк, и он постоянно пополняется, а применение этих лекарств в клинической практике доказывает их эффективность при лечении различных форм рака у взрослых и у детей.
Более подробную информацию о возможности пройти иммунотерапию рака можно получить на нашем сайте, заполнив форму контакта. В течение суток предоставляется бесплатная консультация ведущего онколога, вся необходимая информация и всесторонняя организационная помощь в прохождении лечения в выбранной клинике.
Закажите бесплатную консультацию
Интересные исторические факты иммунотерапии в онкологии
Препараты иммунотерапии – это новое, перспективное и еще недостаточно изученное направление в онкологии, но корнями своими оно уходит к концу 19-го века. Американский хирург Вильям Коли в 1891 г. обнаружил уникальную закономерность у онкологических больных, переболевших стрептококковой инфекцией (рожистым воспалением, скарлатиной). Спустя время после этих инфекций он отметил обратное развитие, уменьшение опухолей, в частности, саркомы. Это побудило его к созданию первой противораковой вакцины на базе ослабленных возбудителей инфекционных заболеваний. При введении в организм они не вызывали развития инфекции, а лишь стимулировали иммунную систему, и образовавшиеся антитела воздействовали на опухоль. Ученый получил серию хороших результатов в лечении рака, но его метод был подвергнут критике как противоестественный и опасный.
Лишь спустя много лет, в 60-е годы прошлого века, с развитием иммунологии и открытием различных факторов иммунитета (интерлейкина, интерферона, факторов роста и т.д.) положило начало системному созданию и применению иммунопрепаратов в онкологии. А с развитием генетики в 1991 г. был выявлен первый онкоген, кодирующий злокачественный рост. В настоящее время таких мутантных генов уже выявлено множество разновидностей и принадлежность их к развитию того или иного вида опухоли. И сами иммунные препараты уже создаются не методом иммунизации человека или лабораторных животных, а методом генной инженерии (перекодирования генов).
Механизм воздействия и основные группы препаратов иммунотерапии
Все современные препараты иммунотерапии в онкологии по механизму действия разделяются на 3 основных группы:
- Создающие активный специфический иммунитет, это противораковые вакцины, содержащие антиген конкретной опухоли и побуждающие организм вырабатывать специфические антитела против нее.
- Неспецифические иммунопрепараты или иммуномодуляторы, повышающие в целом защитные свойства организма, выработку защитных иммунных тел.
- Моноклональные антитела – принципиально новое направление в иммунотерапии рака, это – создание в лабораторных условиях специфических иммунных белковых тел из одной единственной клетки, то есть это специфическая, точечная или клеточная иммунотерапия рака.
Противораковые вакцины для иммунотерапии
Противоопухолевых вакцин создано множество разновидностей, они делятся по способу получения и действия на следующие подгруппы:
-
 клеточные вакцины, в состав которых входят целые опухолевые клетки (аутологичные – данного пациента или аллогенные – другого пациента с подобным видом рака);
клеточные вакцины, в состав которых входят целые опухолевые клетки (аутологичные – данного пациента или аллогенные – другого пациента с подобным видом рака); - антигенные вакцины, действующим фактором которых является лишь антиген, извлеченный из опухолевых клеток.
В клеточных вакцинах содержатся раковые клетки, ослабленные и лишенные способности к развитию и делению, поэтому они не могут «заразить» пациента раком, а лишь вызывают выработку на них иммунных тел. В состав антигенных вакцин входят не целые раковые клетки, а лишь их различные компоненты: белки, генетический материал (ДНК, РНК). Для их введения используются специальные вирусы-проводники, которые не вызывают заболевания, а лишь способствуют транспортировке антигенов к иммунной системе.
Примерами наиболее используемых в практике вакцин являются Oncophage (Витеспен), Onyvax, Cancer-Vax, NY-ESO-1, ALVAC-CEA, VG-1000, TRICOM, Prostvac и другие. Одни из них являются моновалентными, предназначенными для одного вида рака, другие – поливалентными, которые можно применять для лечения нескольких видов рака. Одни вакцины уже широко применяются в клинической практике, целый ряд новых вакцин проходят клинические испытания, постоянно ведется научный поиск и разработка более эффективных вакцин.
Неспецифические иммунопрепараты в онкологии, адьюванты
Эти препараты оказывают общее стимулирующее действие на иммунную систему, и таким образом усиливают в том числе и противораковый иммунитет. Они обычно применяются как адьюванты – дополнение к другим препаратам для усиления выработки специфического противоопухолевого иммунитета.
Наибольшее применение в онкологии получили следующие препараты:
- иммуномодуляторы – Талидомид, Ревлимид, Ромалист, а также бацилла Кальметта-Герена (BCG), то есть то, что нам известно, как БЦЖ – иммунизация ослабленной микобактерией туберкулеза;
- цитокины – белковые молекулы, влияющие на активность иммунных клеток и их деление: Интерлейкин-2, Интерферон-альфа, Колониестимулирующий фактор, Сарграмостин.
Моноклональные антитела в иммунотерапии
Открытие и создание моноклональных антител совершило революцию в иммунотерапии рака. Они представляют собой иммунные белки, вырабатываемые одной клеткой (клоном), потому обладают специфичным направленным действием именно на подобные клетки.
По механизму действия выделяют 2 группы моноклональных антител:
- неконъюгированные – оказывающие самостоятельное воздействие на раковую клетку и «помечающие» опухоль для иммунной системы;
- конъюгированные, или препараты целевого (таргетного) действия, несущие на себе к раковым клеткам молекулы химиопрепарата или же радиоактивные изотопы;
Наиболее широко применяются именно неконъюгированные моноклональные антитела, кроме «указательной» функции они сами воздействуют на клетки рака – угнетают факторы роста, активность ферментов, блокируют ангиогенез (образование новых сосудов в растущей опухоли). Примерами подобных препаратов являются Алемтузумаб для лечения лейкемии за границей, Ритуксимаб для лечения лимфомы, Эрбитукс для лечения рака толстой кишки, Герцептин для лечения рака молочной железы за рубежом, Рамуцирумаб для лечения рака желудка и другие препараты.
Конъюгированные моноклональные антитела – новое направление в комбинированном лечении рака, объединяющее в себе сразу 2 метода: радио- и иммунотерапию и химио- и иммунотерапию. Например, Ибритумомаб (Зевалин), применяемый для лечения лимфомы, Трастузумаб длялечения рака молочной железы.
В настоящее время в США и Европе ведутся работы по созданию поливалентных и гуманизированных моноклональных антител, а также конъюгированных с микроэлементом селеном, повышающим эффективность лечения.
Узнайте точную стоимость лечения
Препараты иммунотерапии для разных видов рака
Препараты иммунотерапии показаны на всех стадиях рака и практически при раке любой локализации. На ранних стадиях рака они сыграют большую роль в предупреждении метастазирования опухоли в лимфоузлы и органы, а также существенно снизят вероятность ее рецидива после лечения, укрепят иммунную систему. На поздних, метастатических стадиях рака они способствуют замедлению развития опухоли и ее распространения, а коньюгированные препараты отыщут вторичные раковые очаги в любом участке организма и проведут таргетное воздействие химиопрепаратом или радиоактивными частицами, непосредственно на клеточном уровне, не повреждая при этом здоровых тканей.
Припараты иммунотерапии при раке легкого
В комплексе лечения рака легких применяются:
- Бевацизумаб (Авастин) – ингибитор ангиогенеза, лишающий опухоль притока крови и приводящий к задержке ее развития, применяется в сочетании с химиопрепаратами, содержащими платину;

- Бавитуксимаб – воздействует на внешнюю белковую защиту раковых клеток и делает их заметными для иммунной системы организма;
- Патритумаб – оказывает блокирующее воздействие на белковый механизм деления раковых клеток, обычно применяется в сочетании с препаратом Эрлотиниб.
Припараты иммунотерапии при раке простаты
Для лечения рака простаты наиболее применяемы следующие препараты:
- Вакцина GVAX – клеточная вакцина, оказывающая блокирующее влияние на рост раковых клеток;
- Вакцина PROSTVAC – изготовлена на основе опухолевого антигена PSA и содержит вирусный «проводник» (из ослабленного вируса оспы кур);
- Вакцина Прованж (Provenge) – терапевтическая клеточная вакцина, изготавливаемая для каждого пациента индивидуально в специальной лаборатории;
- Вакцина ProstAtak – конъюгированная вакцина; содержащая молекулы цитостатика Валацикловира и вирусный проводник для доставки препарата непосредственно раковым клеткам;
- Ипилимумаб (Yervoy) – моноклональное антитело, активизрующее цитотоксическое действие Т-лимфоцитов и повышающее иммунный ответ за счет обнаружения раковых клеток.
Припараты иммунотерапии при раке молочной железы
При раке молочной железы, в основном, применяются вакцины и моноклональные антитела:
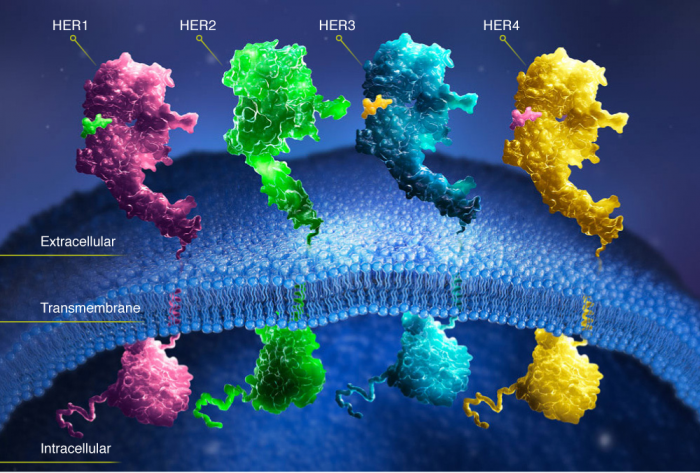
- Герцептин – содержит моноклональные антитела, блокирущие белок HER-2 в раковых клетках, тем самым препятствующие их росту и развитию;
- Вакцина Neuvenge – эффективна при наиболее агрессивном HER-2 позитивном раке груди;
- Вакцина РЕСАН (создана в Беларуси) – включает более 40 разновидностей антигенов опухоли, создает клеточный противораковый иммунитет с формированием «памяти» иммунитета, что значительно снижает число рецидивов рака;
- Тайкерб (Лапатиниб) – оказывает действие, подобное Герцептину, но имеет более широкий спектр эффективности, и применяется в сочетании с Кселодой, когда Герцептин оказывается малоэффективным.
Припараты иммунотерапии при раке желудка
Для лечения рака желудка в комплексе с химиотерапией применяются следующие иммунные препараты:
- Иматиниб (Тайверб) – моноклональное антитело, блокирующее рецепторы роста раковой клетки;
- Бортезомиб (Велкейд) – ингибитор белкового обмена в раковых клетках, повреждает структуру ДНК, повышает чувствительность опухоли к химиотерапевтическим препаратам;
- Эверолимус – препарат применяется как ингибитор иммунитета при пересадке органов, но обнаружено его сильное угнетающее действие на раковые клетки путем блокирования фермента АТФ.
Припараты иммунотерапии меланомы
Одна из самых злокачественных опухолей – меланома, устойчивая ко многим химиопрепаратам, оказалась более «податливой» к воздействию иммунотерапии:
- Ниволумаб – является моноклональным антителом таргетного действия, блокирует рост опухолевых клеток;
- Пембролизумаб (Кейтруда) – моноклональное антитело, блокирует защитный белок PD-1 меланомных клеток, делая их заметными для иммунной системы.
Большой опыт применения подобных препаратов накоплен в лечении рака в Израиле, где эффективность терапии меланомы является самой вкоысой.
Проконсультируйтесь с врачом Online
Где можно пройти лечение рака иммунопрепаратами
Иммунотерапия рака за границей – новый и пока еще дорогостоящий метод лечения рака, тем более, что большинство современных препаратов выпускаются западными фармацевтическими кампаниями. Поэтому, если ваш выбор падает на отечественной онкологии, то такое лечение можно пройти в столицах России, Украины, Казахстана, Беларуси.
Если же вы можете позволить себе лечение за границей, то во всех онкологических центрах развитых стран оно доступно на самом высоком уровне, а цены на лечение рака за рубежом более демократичными будут в клиниках Израиля. Более подробно узнайте обо всем через контактную форму на сайте.
Источник
Вопросами лечения рака желудка занимаются многочисленные лаборатории, ученые, врачи. И последние десятилетия намечается значительный прогресс в этом вопросе, заметный, правда, больше в теории, чем на практике. Для многих больных заявленные прогнозы все еще остаются не вполне благоприятными. Соответственно, на фоне того, что иммунотерапия при лечении различных видов рака, в том числе почки, молочной и предстательной железы все больше специалистов проявляют интерес к вопросам применения этого метода в лечении рака желудка.
Принципы иммунотерапии
Основная задача иммунной системы – различать “чужие” клетки и организмы и изолировать их от “своих”. Соответственно, иммунотерапия предполагает, что с раковыми клетками будет бороться сам иммунитет. Правда, для этого организму необходима определенная помощь. После того, как впервые была выдвинута подобная теория, далеко не все восприняли ее серьезно, некоторые ученые напрочь отвергали даже возможность проведения экспериментов в этой области. Но вскоре способность иммунитета самостоятельно бороться с раковыми клетками была доказана, теория была полностью подтверждена на практике стала неотъемлемой частью системы иммуноредактирования рака.
Весь процесс иммунного ответа условно делят на три фазы. Это фаза устранения, равновесия и избегания. На первом этапе рост клеток опухоли может привести к некоторым изменениям в окружающих зонах, в том числе и к их локальному повреждению. В это же время иммунная система секретирует цикотины и Ɣ-интерфероны и сдерживает процесс образования новых клеток опухоли. Следующий процесс – антигенпрезентирующие дендритные клетки приступают к поглощению опухолевых антигенов, тем самым активируя Т-лимфоциты, которые и отвечают за иммунный ответ.
Самым сложным и продолжительным этапов в иммуноредактировании является этап равновесия. В этой фазе все клетки имеют динамический баланс. Но, так как в это время наблюдается генетическая нестабильность при которой раковые клетки могут быть вполне устойчивыми, они выживают и приобретают резистентность, следствием чего является фаза избегания.
При изучении иммунотерапии значимым этапом был процесс выделения первого антигена опухоли, который бы распознавался Т-клетками. Для этого был клонирован ген MAGE, который, собственно, и кодирует антигены. Эти опыты и доказали саму возможность использования иммунотерапии для лечения рака, заставив клетки иммунной системы самостоятельно находить и уничтожать “чужие” клетки.
Вакцина против рака
Такая вакцина используется для того, чтобы активировать клетки иммунной системы, улучшить ее способности распознавать раковые клетки и уничтожать их, стимулируя опухолеспецифичные Т-лимфоциты. Весь процесс выглядит примерно следующим образом: используя антиген-презентирующие клетки Т-клетки распознают опухолевые антигены. Как правило, антигены имеют довольно специфические признаки, это пептиды, расположенные внутри клетки, но на поверхности клетки имеются молекулы, которые легко распознаются Т-клетками.
В процессе изучения этого вопроса были обследованы несколько тысяч опухолевых антигенов. Но особое внимание привлек именно ген MAGE, который впервые был обнаружен у больных меланомой. Но он может быть представлен в самых различны опухолях, а также на нормальных, здоровых клетках, где ген совершенно не проявляет себя. Остальные возможные антигены являются пептидами, которые возникли вследствие каких-либо мутаций, могут быть представлены антигенами дифференцировки, избыточной экспрессии и вирусные антигены.
При раке желудка MAGE экспрессируется в 38% случаев. При проведении доклинических исследований было выявлено, каким именно образом Helicobacter pilori осуществляет индуцирование экспрессии МАGE-3. Первые опыты проводились на модели рака желудка мышей. Как следствие – была получена регрессия опухоли. На следующем этапе ученые провели исследование на 22 пациентах, имеющих диагноз рак желудка. В этой фазе исследований использовались пептиды VEGF-R1 и VEGF-R2, которые применялись совместно с цисплатиной и S-1. Итоговый результат – частичная регрессия у 55% пациентов, увеличение общей выживаемости. Дополнительно в ходе исследований было выявлено, что опухолевые антигены, которые связаны с HER2/neu, могут значительно повлиять на развитие иммунотерапии и результативность вакцинации против рака.
Еще одним видом иммунотерапии является адоптивная иммунотерапия, при которой у больного выявляют опухолевые Т-клетки и культивируют их вне организма. Затем они возвращаются пациенту уже генетически модифицированные и в несколько увеличенном количестве. В качестве активированных киллеров используются различные типы клеток, среди которых имеются и лимфоциты, особенностью которых является инфильтрация опухолей.
В одном из последних исследований принимали участие 44 больных раком желудка. Для лечения использовались тумор-ассоциированные лимфоциты, в одном случае применялась химиотерапия, а в другом – нет. Более высокая общая выживаемость наблюдалась в группе, где тумор-ассоциированные лимфоциты использовались вместе с химиотерапией. Здесь же была проверена и теория использования цитокин-индуцированных киллеров, которые были обработаны in vitro. Здесь результат был более высокий, чем при использовании только химиотерапии. При этом отмечается, что большое значение имеет специфика обработки киллеров, благодаря чему значительно уменьшается количество побочных эффектов, которые возможны при применении иммунотерапии, в том числе и жизнеугрожающих последствий лечения.
Ингибиторы иммунных контрольных точек
Для того, чтобы снизить негативные последствия от применяемого лечения, требуется регулировать активность Т-клеток. Для этого в процесс лечения включены несколько контрольных точек, помогающих более явно и своевременно определить возможные проблемы. Ингибирующими рецепторами служат CTLA-4 и РD-1, они возникают на поверхности Т-клеток, где после активации они и передают негативный сигнал. Таким образом, осуществляется блокада этих антител, что влияет на активность самих Т-клеток, которые работают при большинстве разновидностей опухолей.
В геномных атласах рака не так давно были определены 4 опухолевых подтипа адекарциномы желудка:
- позитивные по вирусу Эпштейна-Барр;
- микросателлитные нестабильные;
- геномно-стабильные;
- с хромосомой нестабильности.
Использование подобной классификации значительно упрощает работу врача при выборе наиболее эффективного лечения. Так, подгруппа с вирусом Эпштейн-Барр, к которой относится около 15% больных раком желудка, имеет более высокую экспрессию РD-L1. Этот показатель сигнализирует о выраженном присутствии иммунных клеток, а, значит, применение ингибиторов иммунных контрольных точек будет вполне оправданным.
Тремелимумаб
Вторая фаза исследований проходила для 18 больных с раком желудка. В этом случае использовался тремелимумаб. Результат был не столь ожидаемым, но все же с положительной динамикой. Объективный ответ удалось получить лишь у 5% больных, медиана выживаемости в этом случае – 4,8 месяцев.
На основании проведенных исследований возникло предположение, что одновременное использование двух ингибиторов может обеспечить более высокий результат. В итоге был представлен новый препарат MEDI 4736, который является моноканальным антигеном IgG1. Его задача – связаться с РD-L1, препятствуя его соединению с РD-1 и СD-80. Данные, полученные на предварительном этапе, показали отличный результат, с высокой эффективностью препарата при большом количестве различных опухолей, среди которых имеется и рак желудка. На сегодня все еще продолжаются исследования MEDI 4736, используемого в качестве монотерапии и в связке с иммуномодуляторами.
Ниволумаб
Применение Ниволумаба обеспечило достаточно высокую эффективность лечения при многих видах опухоли. Это антитело является хорошим блокатором, который препятствует взаимодействию РD-1 и РD-L1. Этот препарат изначально был одобрен для лечения меланомы (нерезектабельной или метастатической), после прогрессирования при применении ипилимумабе. Несколько позже Ниволумаб одобрили и в качестве препарата для 2-й линии лечения рака легкого. Как показали исследования, Ниволумаб оказался более эффективным по сравнению с доцетакселом при плоскоклеточном немелкоклеточном раке легкого.
Сейчас активно проводятся исследования по применению ниволумаба в качестве самостоятельного препарата или его использование комплексного применения при лечении рака желудка. Первые полученные данные показали, что использование двойной блокады РD-1 и СТLА-4 обеспечивало повышенный выброс цитокинов и приводило к увеличению пролиферации определенных Т-клеток по сравнению с блокадой лишь одного из рецепторов. Соответственно, такие показатели привели к новым этапам исследования, где ниволумаб может использоваться в монотерапии или в комплексе с ипилимумабом при лечении метастатического рака желудка, мелкоклеточного рака легкого и некоторых других видов опухолей.
Пембролизумаб
Еще один из эффективных препаратов для лечения рака – пембролизумаб. Он является гуманизированным моноклональным IgG4 антителом, роль которого – блокировать совместную работу PD-1 с PD-L1 и PD-L2. На этапе исследований этот препарат показал достаточно высокие результаты. У 135 пациентов с метастатической меланомой общий ответ составил 26%,. К тому же, как показали лабораторные исследования применение пембролизумаба имеет управляемый профиль токсичности. В связи с вышеперечисленным, FDA одобрило пембролизумаб как средство для лечения меланомы. После этого были проведены исследования по применению препарата для лечения больных раком желудка. Исследования проводились среди 165 пациентов. Среди них 65 человек были PD-L1 позитивными, больше половины из них (39 человек) каждые 2 недели получали лечение в виде пембролизумаба. И у 41% в итоге отмечается уменьшение опухоли. При этом было проедено некоторое разделение на азиатскую и неазиатскую группы.
Результат азиатской популяции – 32%, неазиатской – 30%. ПО заверению самих больных и их врачей, пациенты достаточно легко перенесли лечение. Важным фактором в этом случае послужило то, что каждый из них предварительно также проходил различные этапы избавления от раковой опухоли, и, как правило, такое лечение было достаточно серьезным.
Подводя итоги
На данный момент иммунотерапия является одним из основных методов лечения многих видов рака. Несмотря на то, что первые прогнозы были вовсе не оптимистичными, результаты проведенных исследований позволили смело заявлять о том, что именно такой метод лечения может стать передовым. Особенно это касается меланомы, где особо отмечено улучшение выживаемости. А вот лечение рака желудку требует дополнительного изучения, проведения лабораторных исследований, тестирований на различных группах и в различных условиях. К тому же, изучение этого вопроса могло бы помочь в выявлении тех биомаркеров, которые были бы максимально эффективны при использовании иммунотерапии. В этом случае возможно увеличение числа пациентов с положительным результатом от применяемого лечения. К тому же, этот метод поможет выявить больных, у которых более вероятно развитие токсичности, а, значит, определить экономическую выгоду от применяемого лечения будет намного проще.
Источник
